Cacodilo
El cacodilo, también conocido como dicacodilo o tetrametildiarsina, (CH3)2As-As(CH3)2, es un compuesto de organoarsénico que constituye una parte importante del líquido fumante de Cadet (llamado así por el químico francés Louis Claude Cadet de Gassicourt). Es un líquido aceitoso venenoso con un olor a ajo extremadamente desagradable. El cacodilo experimenta combustión espontánea en aire seco.
| Cacodilo | ||
|---|---|---|
 | ||
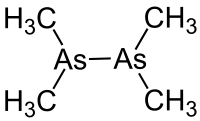 | ||
| Nombre IUPAC | ||
| Tetrametildiarsano | ||
| General | ||
| Otros nombres |
Tetrametildiarsina Tetrametildiarsénico | |
| Fórmula semidesarrollada | (CH3)2As2 | |
| Fórmula molecular | C4H12As2 | |
| Identificadores | ||
| Número CAS | 471-35-2[1] | |
| ChemSpider | 71351 | |
| PubChem | 79018 | |
| Propiedades físicas | ||
| Masa molar | 20 998 g/mol | |
| Punto de fusión | −5 °C (268 K) | |
| Punto de ebullición | 163 °C (436 K) | |
| Peligrosidad | ||
| Frases H | H331H301H410 | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El cacodilo también es el nombre del grupo funcional o radical (CH3)2As.
Síntesis editar
Una mezcla de cacodilo y óxido de cacodilo ((CH3)2As—O—As(CH3)2) fue preparada por Cadet por primera vez a partir de la reacción química del acetato de potasio con trióxido de arsénico. Una reducción posterior produce una mezcla de varios compuestos de arsénico metilados, incluido el dicacodilo. La reacción que forma el óxido sería:
Más tarde se desarrolló una síntesis mucho mejor que comenzó a partir del cloruro de dimetilarsina y dimetilarsina:
Historia editar
Jöns Jakob Berzelius acuñó el nombre kakodyl (en alemán, aunque más tarde se cambió por cacodyl en inglés, y cacodilo en español) para el radical dimetilarsenil, (CH3)2As, palabra que formó del griego kakodes ("maloliente") y hyle ("materia").[2]
Fue investigado por Edward Frankland y durante más de seis años por Robert Bunsen y se considera el compuesto organometálico más antiguo que se haya descubierto (aunque el arsénico no es un metal verdadero).[cita requerida]
Aplicaciones editar
El cacodilo se usaba para tratar de demostrar la teoría radical de Jöns Jacob Berzelius, que generó un aumento en el uso de esta sustancia en los laboratorios de investigación. Posteriormente, el interés en este compuesto tóxico y maloliente disminuyó. Durante la Segunda Guerra Mundial, se consideró su uso como arma química, pero nunca se usó durante la guerra. Los químicos inorgánicos descubrieron sus propiedades como ligando para metales de transición.[cita requerida]
Referencias editar
- ↑ Número CAS
- ↑ Berzelius, J. J. (1839). Jahresberichte über die Fortschritte der physischen Wissenschaften 18: 487.
- John H. Burns and Jürg Waser (1957). «The Crystal Structure of Arsenomethane». J. Am. Chem. Soc. 79 (4): 859-864. doi:10.1021/ja01561a020.
- Seyferth, Dietmar (2001). «Cadet's Fuming Arsenical Liquid and the Cacodyl Compounds of Bunsen». Organometallics 20 (8): 1488-1498. doi:10.1021/om0101947.