Anillo aromático simple
| |||||||||||||||||||||||||||||||||||||||||||||||||
Los anillos aromáticos simples, también conocidos como arenos simples o aromáticos simples, son compuestos orgánicos aromáticos que consisten solo en un sistema de anillo plano conjugado. Muchos anillos aromáticos simples tienen nombres triviales. Por lo general, se encuentran como subestructuras de moléculas más complejas ("aromáticos sustituidos"). Los compuestos aromáticos simples típicos son benceno, indol y piridina.[1][2]
Los anillos aromáticos simples pueden ser heterocíclicos si contienen átomos que no son de carbono, por ejemplo, oxígeno, nitrógeno o azufre. Pueden ser monocíclicos como en el benceno, bicíclicos como en el naftaleno o policíclicos como en el antraceno. Los anillos aromáticos monocíclicos simples suelen ser anillos de cinco miembros como el pirrol o anillos de seis miembros como la piridina. Los anillos aromáticos fusionados consisten en anillos monocíclicos que comparten sus enlaces de conexión.
Anillos aromáticos heterocíclicos editar
Los anillos aromáticos que contienen nitrógeno ( ) se pueden separar en anillos aromáticos básicos que se protonan fácilmente y forman cationes y sales aromáticos (por ejemplo, piridinio) y anillos aromáticos no básicos.
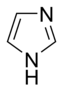
- En los anillos aromáticos básicos, el par solitario de electrones no forma parte del sistema aromático y se extiende en el plano del anillo. Este par solitario es responsable de la basicidad de estas bases nitrogenadas, similar al átomo de nitrógeno en las aminas. En estos compuestos, el átomo de nitrógeno no está conectado a un átomo de hidrógeno. Ejemplos de anillos aromáticos básicos son piridina o quinolina. Varios anillos contienen átomos de nitrógeno tanto básicos como no básicos, por ejemplo, imidazol y purina.
- En los anillos no básicos, el par solitario de electrones del átomo de nitrógeno está deslocalizado y contribuye al sistema aromático de electrones pi. En estos compuestos, el átomo de nitrógeno está conectado a un átomo de hidrógeno. Ejemplos de anillos aromáticos que contienen nitrógeno no básico son pirrol e indol.
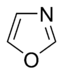
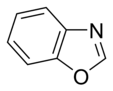
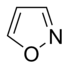
En los anillos aromáticos que contienen oxígeno y azufre, uno de los pares de electrones de los heteroátomos contribuye al sistema aromático (similar a los anillos que contienen nitrógeno no básico), mientras que el segundo par solitario se extiende en el plano del anillo (similar a los anillos primarios que contienen nitrógeno).
Criterios de aromaticidad editar
- La molécula debe ser cíclica.
- Cada átomo del anillo debe tener un orbital p ocupado, que se superpone con los orbitales p en cada lado (completamente conjugado).
- La molécula debe ser plana.
- Debe contener un número impar de pares de electrones pi; debe satisfacer la regla de Hückel: ( ) electrones pi, donde es un número entero que comienza en cero.
Por el contrario, las moléculas con electrones pi son antiaromáticas.
Véase también editar
Referencias editar
- ↑ Clayden, J.; Greeves, N.; Warren, S.; Wothers, P. (2001). Organic Chemistry. Oxford, Oxfordshire: Oxford University Press. ISBN 0-19-850346-6.
- ↑ Eicher, T.; Hauptmann, S. (2003). The Chemistry of Heterocycles: Structure, Reactions, Syntheses, and Applications (2nd edición). Wiley-VCH. ISBN 3-527-30720-6.