Tinción de Gram
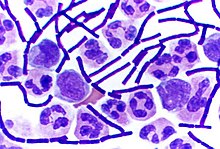
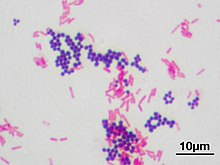
La tinción de Gram o coloración de Gram es un tipo de tinción diferencial empleado en bacteriología para la visualización de bacterias, sobre todo en muestras clínicas. Debe su nombre al bacteriólogo danés Christian Gram (1853-1938), que desarrolló la técnica en 1884.1 Se utiliza tanto para poder referirse a la morfología celular bacteriana como para poder realizar una primera aproximación a la diferenciación bacteriana, considerándose bacterias grampositivas a las que se visualizan de color morado y bacterias gramnegativas a las que se visualizan de color rosado y rojo.



Procedimiento editar
- Recoger muestras para ubicarlas en el microscopio.
- Hacer el extendido con un palillo de madera.
- Dejar secar a temperatura ambiente y fijarlas utilizando un mechero.
- Fijar la muestra con metanol durante un minuto o al calor (flameado tres veces aproximadamente).
- Agregar azul violeta (cristal violeta o violeta de genciana) y esperar un minuto.
- Enjuagar con agua no directamente sobre la muestra.
- Agregar lugol y esperar un minuto aproximadamente.
- Agregar alcohol acetona y esperar entre 5 y 30 segundos según la concentración del reactivo (parte crítica de la coloración). (Las gram - se decoloran, las gram + no).
- Enjuagar con agua destilada.
- Tinción de contraste agregando safranina o fucsina básica y esperar un minuto. Este tinte dejará de color rosado-rojizo las bacterias gram negativas.
- Lavar levemente con agua destilada.
Para observar al microscopio óptico es conveniente hacerlo a 100x con aceite de inmersión.
Explicación editar
El cristal violeta (colorante catiónico) penetra en todas las células bacterianas (tanto gram positivas como gram negativas) a través de la pared bacteriana. El lugol es un compuesto formado por I2 (yodo) en equilibrio con KI (yoduro de potasio), el cual está presente para solubilizar el yodo, y actúa de mordiente, haciendo que el cristal violeta se fije con mayor intensidad a la pared de la célula bacteriana. El I2 entra en las células y forma un complejo insoluble en solución acuosa con el cristal violeta.
La mezcla de alcohol-acetona que se agrega, sirve para realizar la decoloración, ya que en la misma es soluble el complejo I2/cristal violeta. Los organismos gram positivos no se decoloran, mientras que los gram negativos sí lo hacen.
Para poner de manifiesto las células gram negativas se utiliza una coloración de contraste. Habitualmente es un colorante de color rojo, como la safranina o la fucsina. Después de la coloración de contraste las células gram negativas son rojas, mientras que las gram positivas permanecen violetas.
Algunos microorganismos retienen el colorante violeta, aún después de tratarlos con un decolorante, y el color no se modifica al añadir este; otros pierden con facilidad el primer tinte, y toman el segundo. Los que fijan el violeta, se califican de gram positivos, y los que pierden la primera coloración y retienen la segunda, de gram negativos. Basándonos pues, en la reacción gram, podemos clasificar a los microorganismos en uno de los dos grupos. Los colorantes de p-rosanilina son los que mejores resultados dan en la coloración gram. Los representantes más usados de este grupo son violeta de metilo y violeta cristal o de genciana. En realidad, violeta de metilo es el nombre atribuido al compuesto tetrametil-p-rosanilina.
El matiz de color de la p-rosanilina se intensifica al aumentar el número de grupos metilo en la molécula; por consiguiente, de los tres grupos, el tono más oscuro es la hexametil-p-rosanilina (violeta cristal), y el tinte más ligero, la tetrametil-p-rosanilina (violeta de metilo). Los nombres violeta de metilo 3R, 2R, R, B, 2B, 3B, etc., se refieren al número de grupos metilo contenidos. La letra R indica matices rojos, y la letra B, tonos azules. El violeta de cristal contiene seis grupos metilo, y se considera como el mejor colorante primario para teñir por el método de Gram.
La facultad de las células para tomar la coloración gram no es propia de toda sustancia viviente, sino que se limita casi en absoluto a hongos y bacterias. Así vemos que las células de plantas y animales superiores no conservan la primera coloración; los mohos se tiñen con cierta irregularidad; los gránulos de micelios propenden retener el colorante. La reacción de Gram no es infalible ni constante; puede variar con el tiempo del cultivo y el pH del medio, y quizá por otras causas.
Teorías editar
Un microorganismo gram positivo debe presentar una pared celular sana. El mismo microorganismo, si sufre daño de la pared por una u otra causa, se vuelve gram negativo. Esto indica la importancia de la pared para la retención o el escape del colorante. Una posible teoría del mecanismo de tinción es la siguiente:
El colorante básico entra al microorganismo, donde forma con el yodo una laca insoluble en agua. El alcohol o la acetona empleados para aclarar, deshidrata las paredes de los microorganismos gram positivos, tratados con mordiente, y forma una barrera que la laca no puede atravesar. En las células gram negativas, los lípidos de la pared (más abundantes que en las células gram positivas) se disuelven por este tratamiento, lo que permite el escape del complejo de cristal violeta con yodo. Algunos autores objetan esta teoría, pero es indudable la importancia general de la pared celular.
Varias son las teorías emitidas para explicar el mecanismo de la tinción de Gram. Stearn (1923) basó la suya en una combinación química entre el colorante y las proteínas de las bacterias, las proteínas y aminoácidos son cuerpos anfóteros, esto es, tienen la facultad de reaccionar con ácidos y con bases, gracias a sus grupos amino y carboxilo; en soluciones ácidas, reaccionan con los ácidos, y en soluciones alcalinas lo hacen con las bases. De igual manera, comprobaron que la reacción de tinción de las bacterias obedece en gran parte a su contenido proteínico; estos microorganismos se conducen como cuerpos anfóteros, al combinarse con colorantes ácidos en soluciones ácidas y con los básicos en medio alcalino. La combinación con ambos tipos de colorante no se produce en el «punto isoeléctrico». Como los microorganismos contienen más de una proteína, ese punto no tiene un valor preciso y definido, sino que constituye más bien una gama o escala que comprende dos o tres unidades de pH. Según Stern y Stearn, los microorganismos gram positivos tienen una escala isoeléctrica de pH inferior a la de los microorganismos gram negativos; y, a base de sus datos experimentales, deducen las siguientes conclusiones:
- Los microorganismos gram positivos pueden hacerse gram negativos al aumentar la acidez.
- Los microorganismos gram negativos pueden hacerse gram positivos al aumentar la alcalinidad.
- Los microorganismos de reacción positiva a los colorantes ácidos pueden hacerse gram negativos por aumentar la alcalinidad.
- Los microorganismos de reacción positiva a los colorantes básicos pueden hacerse gram negativos por aumentar la acidez.
- En la zona isoeléctrica característica de cada especie es muy escasa la tendencia a retener cualquier colorante.
- Parece estar bien demostrado que las proteínas de las bacterias no son simples, sino más bien una débil combinación de sustancias proteínicas con otras lipoideas o grasas.
- La materia grasa extraída de los microorganismos gram positivos difiere de la obtenida de los microorganismos gram negativos, en que la primera contiene una proporción mucho mayor de ácidos no saturados que muestren gran afinidad por los agentes oxidantes. Todos los mordientes (como el yodo) empleados en la coloración gram son oxidantes; su efecto, en general, consiste en dar a la sustancia oxidada un carácter más ácido. Esto aumenta la afinidad de un microorganismo por los colorantes básicos.
- El cambio de respuesta a la coloración de Gram con el tiempo es propio, sobre todo, de los microorganismos débilmente gram positivos cultivados en los medios que contengan sustancias capaces de fermentar, y cuya reacción se vuelve ácida en el curso del desarrollo.
Gianni (1952) comprobó que las bacterias gram positivas Bacillus subtilis y Bacillus anthracis originaban una reacción negativa cuando los cultivos databan de dos a tres horas. Luego se desarrollaba la sustancia gram positiva debajo de la pared celular y se invertía la reacción. Otra explicación de la reacción de Gram puede ser la posible existencia de una capa exterior alrededor de un núcleo gram negativo. Libenson y Mcllroy, han comunicado que si la reacción gram positiva depende de que se forme una combinación compleja entre los componentes de la coloración de Gram y las proteínas de la pared celular, sería de esperar que las bacterias desintegradas por medios físicos retuviesen este tinte, ya que ese tratamiento no podría cambiar el carácter químico de los materiales de dicha pared. Por el contrario, los gérmenes gram positivos desintegrados pierden su capacidad de retener el colorante primario y no se tiñen
La pared celular de los microorganismos gram positivos y gram negativos es permeable al violeta cristal. Sin embargo, la de los primeros no lo es al complejo de yodo y colorante formado en el interior de la célula. Los resultados experimentales obtenidos con una difusión celular exenta de proteínas, y la escasa solubilidad del complejo de yodo y violeta cristal en alcohol y acetona, parecen sustentar la opinión de que la reacción gram positiva consiste esencialmente en la formación, dentro de la célula, de una cantidad apreciable de complejo de yodo y colorante difícil de eliminar con el disolvente. La pared celular de los microorganismos gram positivos, a diferencia de la de los gram negativos, sería prácticamente impermeable al violeta cristal. Los microorganismos aparecerán teñidos después de tratarlos con violeta cristal, por ser absorbido el colorante en la superficie externa de la pared celular, y el disolvente eliminará sin dificultad el complejo formado después del tratamiento con yodo.
Ni los grupos sulfhidrilo ni las proteínas básicas han influido específicamente en el mecanismo del colorante de Gram. Libenson y Mcllroy han sostenido que la permeabilidad de la pared celular al violeta cristal, la escasa solubilidad del complejo de yodo y colorante en alcohol y acetona, y el libre acceso del disolvente al complejo constituido, son los principales factores que intervienen en el mecanismo de esa coloración.
Bacterias resistentes a la tinción de Gram editar
Las siguientes bacterias de naturaleza gram positiva se tiñen como gram negativas:
- Mycobacterias (están encapsuladas).
- Mycoplasmas (no tienen pared).
- Formas L (pérdida ocasional de la pared).
- Protoplastos y esferoplastos (eliminación total y parcial de la pared, respectivamente).
Utilidades editar
En el análisis de muestras clínicas suele ser un estudio fundamental por cumplir varias funciones:
- Identificación preliminar de la bacteria causal de una infección.
- Utilidad como control calidad del aislamiento bacteriano. Los morfotipos bacterianos identificados en la tinción de Gram se deben de corresponder con aislamientos bacterianos realizados en los cultivos. Si se observan mayor número de formas bacterianas que las aisladas hay que reconsiderar los medios de cultivos empleados así como la atmósfera de incubación.
A partir de la tinción de Gram pueden distinguirse varios morfotipos distintos: Los cocos son de forma esférica. Pueden aparecer aislados después de la división celular (micrococos), aparecer por pares (diplococos), formar cadenas (estreptococos), o agruparse de manera irregular (estafilococos).
Los bacilos poseen forma alargada. En general suelen agruparse en forma de cadena (estreptobacilos) o en empalizada.
También pueden distinguirse los espirales, que se clasifican en espirilos (si son de forma rígida) o espiroquetas (si son blandas y onduladas). Si por el contrario, poseen forma de «coma» (o curvados) entonces se los designa vibrios.
Fundamentos de diferenciación de gram positivo y gram negativo editar
Los fundamentos de la técnica se basan en las diferencias entre las paredes celulares de las bacterias gram positivas y gram negativas
La pared celular de las bacterias gram positivas posee una gruesa capa de peptidoglicano, además de dos clases de ácidos teicoicos: anclado en la cara interna de la pared celular y unido a la membrana plasmática, se encuentra el ácido lipoteicoico, y más en la superficie, el ácido teicoico que está anclado solamente en el peptidoglicano (también conocido como mureína).
Por el contrario, la capa de peptidoglucano de las bacterias gram negativas es delgada, y se encuentra unida a una segunda membrana plasmática exterior (de composición distinta a la interna) por medio de lipoproteínas. Tiene una capa delgada de peptidoglicano unida a una membrana exterior por lipoproteínas. La membrana exterior está hecha de proteína, fosfolípido y lipopolisacárido.
Por lo tanto, ambos tipos de bacterias se tiñen diferencialmente debido a estas diferencias constitutivas de su pared. La clave es el peptidoglicano, ya que es el material que confiere su rigidez a la pared celular bacteriana, y las gram positivas lo poseen en mucha mayor proporción que las gram negativas.
La diferencia que se observa en la resistencia a la decoloración se debe a que la membrana externa de las bacterias gram negativas es soluble en solventes orgánicos, como por ejemplo la mezcla de alcohol/acetona. La capa de peptidoglucano que posee es demasiado delgada como para poder retener el complejo de cristal violeta/yodo que se formó previamente, y por lo tanto este complejo se escapa, perdiéndose la coloración azul-violácea. Por el contrario, las bacterias gram positivas, al poseer una pared celular más resistente y con mayor proporción de peptidoglicanos, no son susceptibles a la acción del solvente orgánico, sino que este actúa deshidratando los poros, cerrándolos, lo que impide que pueda escaparse el complejo cristal violeta/yodo, y manteniendo la coloración azul-violeta.
Factores que alteran la tinción de Gram editar
- Edad de la bacteria.
- Errores del operador.
- Uso de antibióticos
A pesar de la gran utilidad de la tinción de Gram, este método debe ser valorado con precaución, ya que la reacción puede variar según la edad de las células (cultivos viejos de bacterias gram positivas pueden perder capas de peptidoglicanos y teñirse como gram negativos) y la técnica empleada (al decolorar por un tiempo muy prolongado se puede correr el riesgo que bacterias gram positivas se tiñan como gram negativas). Por esta situación, junto a la muestra deben teñirse controles con bacterias gram positivas (por ejemplo, Staphylococcus aureus) y gram negativas (por ejemplo, Escherichia coli).
Bibliografía editar
1.-Gram, C. (1884). The differential staining of Schizomycetes in tissue sections and in dried preparations. Fortschritte der Medizin, 2, 185-9. Disponible en https://web.archive.org/web/20160610220109/http://www.asmusa.org/ccLibraryFiles/FILENAME/0000000235/1884p215.pdf.
2.-Aulton Michael E. (2004): Ciencia y diseño de formas farmacéuticas. España: Elsevier, segunda edición, 2004.
3.-Bergey, David H.; Holt, John G.; Krieg, Noel R.; Sneath, Peter H. A. (1994): Bergey's manual of determinative bacteriology. Lippincott Williams & Wilkins, novena edición, 1994. ISBN 0-683-00603-7.
4.-Madigan, M. T; Martinko J., Parker J. (2004): Brock biology of microorganisms. Lippincott Williams & Wilkins, décima edición, 2004. ISBN 0-13-066271-2.
5.-Søgaard, M.; Nørgaard, M.; Schønheyder, H. (2007): «First notification of positive blood cultures: high accuracy of the Gram stain report», artículo en la revista Journal of Clinical Microbiology, 45: pág. 1113; 2007.