Glutatión
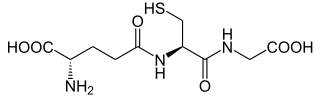
El glutatión (también glutationa) (GSH)[2] es un tripéptido constituido por los aminoácidos glutamato, cisteína y glicina. Contiene un enlace peptídico inusual entre el grupo amino de la cisteína y el grupo carboxilo de la cadena lateral del glutamato.
Se trata del principal antioxidante de las células, es ubicuo y ayuda a protegerlas de las especies reactivas del oxígeno, como los radicales libres y los peróxidos.[3]
La reducción de GSh es un péptido molecular pequeño. Una gran cantidad de péptidos en los organismos vivos, especialmente en las células hepáticas, protegen la membrana de las células hepáticas, promueven el ejercicio de la actividad de las enzimas hepáticas y se combinan con una variedad de productos químicos tóxicos para desintoxicar.[4] Es nucleofílico en azufre y ataca los aceptores conjugados electrofílicos venenosos. Los grupos tiol se mantienen en un estado reducido a una concentración de aproximadamente ~ 5 mM en células animales. En efecto, el glutatión reduce cualquier enlace disulfuro formado dentro de proteínas citoplasmáticas de cisteínas, al actuar como un donante de electrones. En el proceso, el glutatión se convierte en su forma oxidada, llamada disulfuro de glutatión (GSSG). En las células, el glutatión se encuentra principalmente en su estado reducido (GSH) y, en mucha menor proporción, en su estado oxidado (GSSG).
| Glutatión | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| Ácido(2S)-2-Amino-4-{[(1R)-1-[(carboximetil)carbamoil]-2-sulfaniletil]carbamoil}butanoico | ||
| General | ||
| Fórmula estructural |
| |
| Fórmula molecular | C10H17N3O6S | |
| Identificadores | ||
| Número CAS | 70-18-8[1] | |
| ChEBI | 60836 | |
| ChEMBL | 1543 | |
| ChemSpider | 111188 | |
| DrugBank | DB00143 | |
| PubChem | 124886 | |
| UNII | GAN16C9B8O | |
| KEGG | C00051 | |
|
C(CC(=O)N[C@@H](CS)C(=O)NCC(=O)O)[C@@H](C(=O)O)N
| ||
| Propiedades físicas | ||
| Masa molar | 307,084 g/mol | |

Ello es así ya que la enzima que "reduce" el tripéptido a partir de su forma oxidada, la glutatión reductasa, es constitutivamente activa e inducible en situaciones de estrés oxidativo. De hecho, la proporción GSH/GSSG dentro de las células se utiliza a menudo como "indicador" del estado oxidativo de la célula y de la toxicidad celular.[5]
- H2O2 + 2GSH------- GSSG + 2 H2O
Biosíntesis editar
El glutatión no es un nutriente esencial, ya que se puede sintetizar a partir de los aminoácidos: cisteína (Cys/C), ácido glutámico (Glu/E) y glicina (Gly/G) su fórmula Cys-Glu-Gly o C-E-G.
El sulfhidrilo (tiol), grupo (SH) de la cisteína, sirve como donador de electrones y es responsable de la actividad biológica del glutatión. La prestación de este aminoácido es el factor limitante en la síntesis de glutatión en las células, porque la cisteína es rara en los productos alimenticios. Por otra parte, si se libera, como el aminoácido libre, la cisteína es tóxica y de manera espontánea cataboliza en el tracto gastrointestinal y el plasma de la sangre.[6]
El glutatión se sintetiza en dos pasos dependientes del trifosfato de adenosina:
- En primer lugar, la gamma-glutamilcisteína se sintetiza a partir del L-glutamato y la cisteína a través de la enzima gamma-glutamilcisteína sintetasa (también conocida como ligasa glutamato-cisteína (GCL) ligasa). Esta reacción es el paso limitante en la síntesis de glutatión.
- En segundo lugar, la glicina se añade a la terminal C de la gamma-glutamilcisteína, a través de la enzima glutatión sintetasa.
En animales e insectos, la glutamato cisteína ligasa (GCL) es una enzima heterodimérica compuesta por un catalizador (GCLC) y subunidad moduladora (GCLM). El GCLC constituye toda la actividad enzimática, mientras que la GCLM aumenta la eficiencia catalítica del GCLC. Los ratones que carecen de GCLC (es decir, todas las síntesis de nuevo GSH) mueren antes de nacer.[7] Los ratones que carecen de GCLM no demuestran fenotipo, pero exhiben una marcada disminución de GSH y una mayor sensibilidad a los tóxicos.[8][9][10]
Aunque todas las células del cuerpo humano son capaces de sintetizar el glutatión, se ha demostrado que la síntesis de glutatión del hígado es esencial. Después del nacimiento, los ratones con pérdida genética inducida de GCLC (es decir, la síntesis de GSH) sólo en el hígado mueren al cabo de un mes del nacimiento.[11]
La glutamato cisteína ligasa de las plantas (GCL) es una enzima redox homodimérica sensible, conservada en el reino vegetal.[12] En un ambiente oxidante, se forman puentes disulfuro intermoleculares, y la enzima cambia al estado dimérico activo. El potencial crítico medio de la parella de cisteína es de -318 mV.
Además del control redox, está la enzima GCL inhibida por GSH.[13] La GCL se encuentra únicamente en los plastidios, y la glutatión sintetasa se halla en los plastidios y en el citosol; por lo tanto, son exportados (GSH y gamma-glutamilcisteína) de los plastidios.[14] Las dos biosíntesis de las enzimas del glutatión son esenciales en las plantas.[15]
La ruta de biosíntesis del glutatión se encuentra en algunas bacterias, como las cianobacterias y proteobacterias, pero está ausente en muchas otras. La mayoría de los organismos eucariotas sintetizan glutatión, incluidos los seres humanos, pero algunos no, como las leguminosas, Entamoeba y Giardia.[16][17]
Función editar
En el estado reducido, el grupo tiol de la cisteína es capaz de donar un equivalente de reducción (H+ + e-) a otras moléculas inestables, tales como las especies reactivas de oxígeno. Al donar un electrón, el glutatión se convierte en reactivo, pero se combina rápidamente con otro glutatión reactivo para formar disulfuro de glutatión (GSSG). Esta reacción es posible debido a que el glutatión se encuentra en una proporción relativamente alta en las células (de hasta 5 mM, en los hepatocitos). El GSH puede regenerarse a partir de GSSG por medio de la enzima glutatión reductasa.
En las células y tejidos sanos, más del 90 por ciento de glutatión total se encuentra en la forma reducida (GSH) y menos del 10 por ciento se encuentra en la forma disulfuro (GSSG). Un aumento de la proporción entre GSSG y GSH se considera un indicativo de estrés oxidativo.
El glutatión tiene múltiples funciones:
- Es el mayor antioxidante endógeno producido por las células, participa directamente en la neutralización de radicales libres y compuestos de oxígeno reactivo, así como en el mantenimiento de los antioxidantes exógenos; por ejemplo, las vitaminas C y E, en sus formas reducidas (activas).
- A través de la conjugación directa, desintoxica muchos xenobióticos (compuestos extraños) y agentes carcinógenos, tanto orgánicos como inorgánicos.
- Es esencial para que el sistema inmunitario pueda ejercer todo su potencial; por ejemplo, en la modulación de la presentación de antígenos a los linfocitos, lo que influye en la producción de citoquinas y el tipo de respuesta (celular o humoral) que se desarrolla; es capaz de aumentar la proliferación de los linfocitos, lo que aumenta la magnitud de la respuesta, también aumentar la actividad de eliminación de las células T citotóxicas y las células NK, y la regulación de la apoptosis, manteniendo así el control de la respuesta inmune.
- Desempeña un papel fundamental en numerosas reacciones metabólicas y bioquímicas tales como la síntesis y reparación del ADN, la síntesis de proteínas, la síntesis de prostaglandinas, el transporte de aminoácidos y la activación de enzimas. Por lo tanto, todos los sistemas del organismo pueden verse afectados por el estado del sistema glutatión, especialmente el sistema inmunitario, el sistema nervioso, el sistema gastrointestinal y los pulmones.
Función en los animales editar
El GSH es conocido como un sustrato en las dos reacciones de conjugación y las reacciones de reducción, catalizadas por la glutatión S-transferasa, enzima presente en el citosol, en los microsomas y en las mitocondrias. Sin embargo, también es capaz de participar en la conjugación no enzimática de algunos productos químicos, como en el caso de la N-acetil-p-benzoquinona imina (NAPQI), el metabolito reactivo formado por la acción del sistema citocromo P450 sobre el paracetamol (o acetaminofeno, como se conoce en los Estados Unidos). Este metabolito tóxico es el responsable del daño hepático y renal causado por la sobredosis de paracetamol cuando se agota el GSH.
El glutatión se conjuga con NAPQI y facilita la detoxificación del compuesto. Esta capacidad protege los grupos tiol celulares, que de lo contrario se modificarían covalentemente. Cuando todo el GSH se ha consumido, la NAPQI comienza a reaccionar con las proteínas celulares, matando a las células en el proceso. El tratamiento que se prefiere para una sobredosis de este analgésico es la administración (por lo general en forma atomizada) de N-acetil-L-cisteína, que se procesa en las células a L-cisteína y se utiliza en la síntesis de novo de GSH.
El glutatión (GSH) participa en la síntesis de los leucotrienos y es un cofactor de la enzima glutatión peroxidasa. También es importante como una molécula hidrofílica que se añade a las toxinas lipofílicas y residuos en el hígado durante la biotransformación antes de que puedan formar parte de la bilis. El glutatión también es necesario para la desintoxicación del metilglioxal, una toxina producida como un subproducto del metabolismo.
Esta reacción de desintoxicación se lleva a cabo por el sistema glioxalasa. La glioxalasa I cataliza la conversión de glutatión metilglioxal y glutatión reducido a SD-lactoil-glutatión. La glioxalasa II cataliza la hidrólisis de la SD-lactoil-glutatión a glutatión y ácido D-láctico.
El glutatión se ha utilizado recientemente como inhibidor de melanina en la industria cosmética. En países como Filipinas, este producto se vende como jabón blanqueador. El glutatión inhibe competitivamente la síntesis de melanina en la reacción de la tirosinasa y la L-dopa mediante la interrupción de la capacidad de la L-DOPA para unirse a la tirosinasa durante la síntesis de melanina. La inhibición de la síntesis de melanina se ve contrarrestada por el aumento de la concentración de L-DOPA, pero no por el aumento de la tirosinasa.[18]
Función en las plantas editar
En las plantas, el glutatión es crucial para el manejo del estrés biótico y abiótico. Es un componente fundamental del ciclo del glutatión-ascorbato, sistema que reduce el peróxido de hidrógeno[19] tóxico. Es el precursor de las fitoquelatinas, oligómeros del glutatión que quelan metales pesados como el cadmio.[20] El glutatión es necesario para la defensa contra los patógenos de plantas como Pseudomonas syringae y Phytophthora brassicae.[21] La APS reductasa, una enzima de la vía de asimilación de azufre, utiliza glutatión como donante de electrones. Otra enzima que utiliza glutatión como sustrato es la glutarredoxina. Estas pequeñas oxidorreductasas están implicadas en el desarrollo de las flores, el ácido salicílico y la señalización de defensa de la planta.[22]
La suplementación editar
La suplementación ha sido difícil, ya que la investigación sugiere que el glutatión por vía oral no se absorbe bien a través del tracto gastrointestinal. En un estudio de la administración oral aguda de una dosis muy grande (3 gramos) de glutatión, Witschi y su equipo encontraron que "no es posible aumentar la circulación de glutatión en un grado clínicamente beneficioso con la administración oral de una dosis única de 3 g de glutatión."[23][24] No obstante, ya a finales de los años 70, Israil Brekhman (uno de los padres de los adaptógenos) y Raimundo Torres Díaz crearon unas composiciones actualmente llamadas Reactor-20 y Riendol, que hacen llegar el glutatión a través de la vía alveolar-pulmonar, lo cual equivale a una inyección en vena, ya que estos productos pasan de inmediato al torrente sanguíneo y los efectos positivos son muy superiores a los que se administran por vía oral, ya que en la función digestivo-intestinal se pierden mucho de los componentes. Brekhman y Torres fueron los creadores de los inmunoterápicos adaptógenos cubanos, en 1977.[cita requerida]
Sin embargo, las concentraciones plasmáticas y del hígado de glutatión pueden recuperarse con la administración oral de S-adenosil-metionina (SAM)[25][26][27] Los precursores de glutatión ricos en cisteína incluyen N-acetilcisteína (NAC)[28][29] y proteína del suero sin desnaturalizar,[30][31][32][33][34][35][36][37] y se ha demostrado que estos suplementos aumentan el contenido de glutatión de la célula. La N-acetilcisteína está disponible como un medicamento y como un suplemento genérico. También se ha demostrado que el ácido alfa lipoico restaura el glutatión intracelular.[38][39] Y que la melatonina estimula una enzima relacionada, la glutatión peroxidasa.[40] También, que la silimarina, componente del Silybum marianum (cardo mariano), puede llegar a reponer los niveles de glutatión. De todos estos métodos, los dos métodos que más se investigan para la eficacia en el aumento del glutatión intracelular son variantes de la cisteína. Se ha demostrado que la N acetil cisteína, que es un fármaco sobre la lucha contra las drogas, y la cisteína consolidada como se encuentra en los nutracéticos de la proteína del suero sin desnaturalizar son eficaces en el aumento de los valores de glutatión.[41][42]
El glutatión es un componente intracelular fuertemente regulado y limitado en su producción debido a la inhibición de retroalimentación negativa de su propia síntesis a través de la enzima gamma-sintetasa glutamilcisteína. Así, en gran medida, se reduce al mínimo cualquier posibilidad de sobredosis. El aumento de glutatión es una estrategia para hacer frente a los estados de deficiencia de glutatión, el alto estrés oxidativo, la deficiencia inmune y la sobrecarga de xenobióticos (el glutatión participa en la desintoxicación de xenobióticos). Los estados de deficiencia de glutatión incluyen, entre otros: VIH/sida, la química y la hepatitis infecciosa, el cáncer de próstata y otros tipos de cáncer, las cataratas, la enfermedad de Alzheimer, la enfermedad de Parkinson, la enfermedad pulmonar obstructiva crónica, el asma, el envenenamiento por radiación, los estados de malnutrición, el estrés físico arduo, el envejecimiento, y se ha asociado también con una subrespuesta inmune óptima. Muchas patologías clínicas están asociadas con el estrés oxidativo y se detallan en numerosas referencias médicas.[6]
El nivel de glutatión bajo también está fuertemente implicado en el desgaste y el balance[43] negativo de nitrógeno; en particular, se ve en el cáncer, el sida, la sepsis, los traumatismos, las quemaduras e incluso el sobreentrenamiento deportivo. La administración oral de N-acetil cisteína (NAC), un profármaco usado para aumentar los niveles de glutatión después de una sobredosis de acetaminofén, incrementa los niveles de glutatión en pacientes infectados con VIH y ha sido asociado con una supervivencia más prolongada de ellos.[44]
Cáncer editar
Las concentraciones de glutatión en las células tumorales son altas y este puede ser un factor importante en la resistencia a la quimioterapia.[45]
Estudios preliminares han demostrado que el estado de los antioxidantes puede afectar la tolerancia de los niños con leucemia linfoblástica a la quimioterapia. También los inmunoterápicos-adaptógenos-cubanos, desarrollados a finales de los años 70 por Israil Brekhman y Raimundo Torres Díaz (actualmente autorizados por Bruselas para toda la Comunidad Europea y muy empleados por la Asociación de Afectados por las Quimioterapias y Radioterapia, son los que mayor contenido tienen de glutatión a nivel mundial, ya que incorpora también los precursores (cisteína, glicina y ácido glutámico) y los que tienen más de 30 años de pruebas sobre el ser humano. De cualquier manera, hace falta evidencia más concluyente.[46][47][48]
Se realizó un ensayo in vitro en cinco pacientes que cursaban con cáncer de mama con metástasis, uno con cáncer de páncreas y uno con cáncer de hígado, a quienes se les administró 30 g de un concentrado de suero de leche de vaca diariamente durante seis meses.[49]
Patología editar
El exceso de glutamato en las sinapsis, que puede liberarse en condiciones tales como en una lesión cerebral traumática, puede impedir la absorción de cisteína, un componente necesario del glutatión. Sin la protección de la lesión oxidativa otorgada por el glutatión, las células pueden dañarse o destruirse.[50]
Métodos para determinar el glutatión editar
El glutatión reducido se puede rociar con reactivo de Ellman o derivados de bímano, como el monobromobimán. El método monobromobimán es más sensible. En este procedimiento, se lisan las células y tioles extraídos mediante un buffer de ácido clorhídrico. Posteriormente, los tioles se reducen con TDT y se etiquetan con monobromobimán. El monobrombimán se vuelve fluorescente tras su unión al GSH. Los tioles se separan por HPLC, y la fluorescencia puede cuantificarse con un detector de fluorescencia. El bímano también puede utilizarse para cuantificar el glutatión in vivo. La cuantificación se realiza por CLSM después de la aplicación del colorante a las células vivas.[51] El otro enfoque, que permite medir el potencial redox del glutatión con una resolución espacial y temporal en las células vivas, se basa en las imágenes redox utilizando la proteína verde fluorescente sensible al redox (roGFP).[52]
Véase también editar
Referencias editar
- ↑ Número CAS
- ↑ [Merck Index], 11th Edition, 4369.
- ↑ Pompella, A., Visvikis, A., Paolicchi, A., De Tata, V., Casini, A. F. (octubre de 2003). «The changing faces of glutathione, a cellular protagonist». Biochem Pharmacol. 66 (8): 1499-503. PMID 14555227. doi:10.1016/S0006-2952(03)00504-5.
- ↑ «Glutathione».
- ↑ Pastore, A., Piemonte, F., Locatelli, M., Lo Russo, A., Gaeta, L. M., Tozzi, G., Federici, G. (octubre de 2003). «Determination of blood total, reduced, and oxidized glutathione in pediatric subjects». Clin. Chem. 47 (8): 1467-1469. PMID 11468240. Archivado desde el original el 28 de abril de 2009. Consultado el 15 de diciembre de 2009.
- ↑ a b «Immunocal Powder Sachets patient advice including side effects». Archivado desde el original el 19 de agosto de 2010. Consultado el 15 de diciembre de 2009.
- ↑ Dalton, TP; et al., M. Z.; Yang, Y.; Shertzer, H. G.; Nebert, D. W. (2000). «Knockout of the Mouse Glutamate Cysteine Ligase Catalytic Subunit (Gclc) Gene: Embryonic Lethal When Homozygous, and Proposed Model for Moderate Glutathione Deficiency When Heterozygous». Biochem Biophys Res Commun. 279 (2): 324. PMID 11118286. doi:10.1006/bbrc.2000.3930.
|apellido1=y|apellido=redundantes (ayuda);|nombre1=y|nombre=redundantes (ayuda) - ↑ Yang, Y.; Dieter, M. Z.; Chen, Y.; Shertzer, H. G.; Nebert, D. W.; Dalton, TP (2002). «Initial Characterization of the Glutamate-Cysteine Ligase Modifier Subunit Gclm(-/-) Knockout Mouse. NOVEL MODEL SYSTEM FOR A SEVERELY COMPROMISED OXIDATIVE STRESS RESPONSE». J Biol Chem 277 (51): 49446. PMID 12384496. doi:10.1074/jbc.M209372200.
- ↑ Giordano, G., G.; Afsharinejad, Z.; Guizzetti, M.; Vitalone, A.; Kavanagh, T. J.; Costa, L. G. (2007). «Organophosphorus insecticides chlorpyrifos and diazinon and oxidative stress in neuronal cells in a genetic model of glutathione deficiency». Toxicol Appl Pharmacol 219 (2-3): 181. PMID 17084875. doi:10.1016/j.taap.2006.09.016.
|apellido1=y|autor=redundantes (ayuda) - ↑ McConnachie, L. A., Mohar. I., Hudson, F. N. (octubre de 2007). «Glutamate cysteine ligase modifier subunit deficiency and gender as determinants of acetaminophen-induced hepatotoxicity in mice». Toxicol Sci. 99 (2): 628-36. PMID 17584759. doi:10.1093/toxsci/kfm165.
- ↑ Chen, Y., Y.; Yang, Y.; Miller, M. L.; Shen, D.; Shertzer, H. G.; Stringer, K. F.; Wang, B.; Schneider, S. N. et al. (2007). «Hepatocyte-specificGclc deletion leads to rapid onset of steatosis with mitochondrial injury and liver failure». Hepatology 45 (5): 1118. PMID 17464988. doi:10.1002/hep.21635.
|apellido1=y|autor=redundantes (ayuda); - ↑ Hothorn M, Wachter A, Gromes R, Stuwe T, Rausch T, Scheffzek K (septiembre de 2006). «Structural basis for the redox control of plant glutamate cysteine ligase.». J Biol Chem 15 (37): 27557-65. PMID 16766527. doi:10.1074/jbc.M602770200.
- ↑ Hicks, L. M., Cahoon R. E., Bonner, E. R., Rivard, R. S., Sheffield, J., Jez, J. M. (agosto de 2007). «Thiol-based regulation of redox-active glutamate-cysteine ligase from Arabidopsis thaliana.». Plant Cell 19 (8): 2653-61. PMC 2002632. PMID 17766407. doi:10.1105/tpc.107.052597.
- ↑ Wachter, A., Wolf, S., Steininger, H., Bogs, J., Rausch, T. (enero de 2005). «Differential targeting of GSH1 and GSH2 is achieved by multiple transcription initiation: implications for the compartmentation of glutathione biosynthesis in the Brassicaceae.». Plant J 41 (1): 15-30. PMID 15610346. doi:10.1111/j.1365-313X.2004.02269.x.
- ↑ Pasternak, M., Lim, B., Wirtz, M., Hell, R., Cobbett, C. S., Meyer, A. J. (marzo de 2008). «Restricting glutathione biosynthesis to the cytosol is sufficient for normal plant development.». Plant J 53 (6): 999-1012. PMID 18088327. doi:10.1111/j.1365-313X.2007.03389.x.
- ↑ Shelley D. Copley and Jasvinder K. Dhillon (2002). «Lateral gene transfer and parallel evolution in the history of glutathione biosynthesis genes» (free full text). Genome biology 3: research0025.1. doi:10.1186/gb-2002-3-5-research0025. Archivado desde el original el 5 de junio de 2008. Consultado el 15 de diciembre de 2009.
- ↑ Grill D, Tausz T, De Kok LJ (2001). Significance of glutathione in plant adaptation to the environment. Springer. ISBN 1402001789.
- ↑ «[Inhibitory mechanism of melanin synthesis by glut... [Yakugaku Zasshi. 2008] - PubMed result».
- ↑ Noctor G, Foyer CH (junio de 1998). «ASCORBATE AND GLUTATHIONE: Keeping Active Oxygen Under Control». Annu Rev Plant Physiol Plant Mol Biol 49: 249-279. PMID 15012235. doi:10.1146/annurev.arplant.49.1.249.
- ↑ Suk-Bong Ha, Aaron P. Smith, Ross Howden, Wendy M. Dietrich, Sarah Bugg, Matthew J. O'Connell, Peter B. Goldsbrough, and Christopher S. Cobbett (1999). «Phytochelatin Synthase Genes from Arabidopsis and the Yeast Schizosaccharomyces pombe». Plant Cell 11 (6): 1153-1164. PMC 144235. PMID 10368185. doi:10.1105/tpc.11.6.1153.
- ↑ Parisy V, Poinssot B, Owsianowski L, Buchala A, Glazebrook J, Mauch F (enero de 2007). «Identification of PAD2 as a gamma-glutamylcysteine synthetase highlights the importance of glutathione in disease resistance of Arabidopsis.». Plant J. 49 (1): 159-72. PMID 17144898. doi:10.1111/j.1365-313X.2006.02938.x.
- ↑ Rouhier N, Lemaire SD, Jacquot JP (2008). «The role of glutathione in photosynthetic organisms: emerging functions for glutaredoxins and glutathionylation». Annu Rev Plant Biol 59: 143-66. PMID 18444899. doi:10.1146/annurev.arplant.59.032607.092811.
- ↑ Witschi A, Reddy S, Stofer B, Lauterburg BH (1992). «The systemic availability of oral glutathione». Eur J Clin Pharmacol. 43 (6): 667-9. PMID 1362956. doi:10.1007/BF02284971.
- ↑ AIDS Line Update Archivado el 4 de abril de 2007 en Wayback Machine.
- ↑ Liber CS (noviembre de 2002). «S-Adenosyl-L-methionine: its role in the treatment of liver disorders». Am J Clin Nutr. 76 (5): 1183S-1187S. PMID 12418503.
- ↑ Vendemiale G, Altomare E, Trizio T, Le Grazie C, Di Padova C, Salerno MT, Carrieri V, Albano O. (mayo de 1989). «Effects of oral S-adenosyl-L-methionine on hepatic glutathione in patients with liver disease». Scand J Gastroenterol. 24 (9): 407-15. PMID 2781235. doi:10.3109/00365528909093067.
- ↑ Loguercio C, Nardi G, Argenzio F, Aurilio C, Petrone E, Grella A, Del Vecchio Blanco C, Coltorti M. (septiembre de 1994). «Effect of S-adenosyl-L-methionine administration on red blood cell cysteine and glutathione levels in alcoholic patients with and without liver disease». Alcohol Alcohol. 29 (5): 597-604. PMID 7811344.
- ↑ Acetylcysteine and glutathione, PubMed
- ↑ Gross CL, Innace JK, Hovatter RC, Meier HL, Smith WJ (1993). «Biochemical manipulation of intracellular glutathione levels influences cytotoxicity to isolated human lymphocytes by sulfur mustard». Cell Biol. Toxicol. 9 (3): 259-67. PMID 8299004. doi:10.1007/BF00755604.
- ↑ «Glutathione information for Physicians». Archivado desde el original el 28 de abril de 2007. Consultado el 16 de diciembre de 2009.
- ↑ Micke P, Beeh KM, Schlaak JF, Buhl R (febrero de 2001). «Oral supplementation with whey proteins increases plasma glutathione levels of HIV-infected patients». Eur. J. Clin. Invest. 31 (2): 171-8. PMID 11168457. doi:10.1046/j.1365-2362.2001.00781.x.
- ↑ Moreno YF, Sgarbieri VC, da Silva MN, Toro AA, Vilela MM (febrero de 2006). «Features of whey protein concentrate supplementation in children with rapidly progressive HIV infection». J. Trop. Pediatr. 52 (1): 34-8. PMID 16014759. doi:10.1093/tropej/fmi074.
- ↑ Grey V, Mohammed SR, Smountas AA, Bahlool R, Lands LC (diciembre de 2003). «Improved glutathione status in young adult patients with cystic fibrosis supplemented with whey protein». J. Cyst. Fibros. 2 (4): 195-8. PMID 15463873. doi:10.1016/S1569-1993(03)00097-3.
- ↑ Micke P, Beeh KM, Buhl R (febrero de 2002). «Effects of long-term supplementation with whey proteins on plasma glutathione levels of HIV-infected patients». Eur J Nutr 41 (1): 12-8. PMID 11990003. doi:10.1007/s003940200001.
- ↑ Bounous G, Baruchel S, Falutz J, Gold P (junio de 1993). «Whey proteins as a food supplement in HIV-seropositive individuals». Clin Invest Med 16 (3): 204-9. PMID 8365048.
- ↑ Bounous G, Gold P (agosto de 1991). «The biological activity of undenatured dietary whey proteins: role of glutathione». Clin Invest Med 14 (4): 296-309. PMID 1782728.
- ↑ Bounous et al. Multiple references on glutathione enhancement with bioactive whey protein in multiple disease states
- ↑ Shay KP, Moreau RF, Smith EJ, Smith AR, Hagen TM (2009). «Alpha-lipoic acid as a dietary supplement: Molecular mechanisms and therapeutic potential». Biochim Biophys Acta. 1790 (Aug 4): 1149-60. PMC 2756298. PMID 19664690. doi:10.1016/j.bbagen.2009.07.026.
- ↑ Busse E, Zimmer G, Schopohl B, Kornhuber B. (1992). «Influence of alpha-lipoic acid on intracellular glutathione in vitro and in vivo». Arzneimittelforschung. 42 (6): 829-31. PMID 1418040.
- ↑ Barlow-Walden LR, Reiter RJ, Abe M, Pablos M, Menendez-Pelaez A, Chen LD, Poeggeler B. (1995). «Melatonin stimulates brain glutathione peroxidase activity». Neurochem Int. 26 (5): 497-502. PMID 7492947. doi:10.1016/0197-0186(94)00154-M.
- ↑ Nencini C, Giorgi G, Micheli L (2007). «Protective effect of silymarin on oxidative stress in rat brain». Phytomedicine. 14 (2-3): 129-35. PMID 16638633. doi:10.1016/j.phymed.2006.02.005.
- ↑ Valenzuela A, Aspillaga M, Vial S, Guerra R (1989). «Selectivity of silymarin on the increase of the glutathione content in different tissues of the rat». Planta Med. 55 (5): 420-2. PMID 2813578. doi:10.1055/s-2006-962056.
- ↑ Dröge W, Holm E. (1997). «Role of cysteine and glutathione in HIV infection and other diseases associated with muscle wasting and immunological dysfunction». FASEB J. 11 (13): 1077-89. PMID 9367343.
- ↑ Herzenberg LA, De Rosa SC, Dubs JG, Roederer M, Anderson MT, Ela SW, Deresinski SC, Herzenberg LA (1997). «Glutathione deficiency is associated with impaired survival in HIV disease». Proc Natl Acad Sci USA. 94 (5): 1967-72. PMC 20026. PMID 9050888. doi:10.1073/pnas.94.5.1967.
- ↑ Kennedy, R. S., Konok, G. P., Bounous, G., Baruchel, S., Lee, T. D. (1995). The use of a whey protein concentrate in the treatment of patients with metastatic carcinoma: a phase I-II clinical study. PMID 8669840.
- ↑ Kelly, Kara M. (Feb de 2008). Bringing evidence to complementary and alternative medicine in children with cancer: Focus on nutrition-related therapies. pp. 490-3; discussion 498. PMID 18064645.
- ↑ Physician Desk Reference, pdr.net. Immunocal. pp. http://www.pdr.net/full-prescribing-information/immunocal?druglabelid=257.
- ↑ Bodylogic, Estar bien, Sentirse bien. Glutacal, linea nutrición. pp. http://www.bodylogicglobal.com.
- ↑ Balendiran, G.K., Dabur, R., Fraser D. (2004). The role of glutathione in cancer. pp. https://www.ncbi.nlm.nih.gov/pubmed/15386533. PMID 15386533.
- ↑ Pereira C.F, de Oliveira C.R. (Jul de 2000). «Oxidative glutamate toxicity involves mitochondrial dysfunction and perturbation of intracellular Ca2+ homeostasis». Neuroscience Research 37 (3): 227-36. PMID 10940457. doi:10.1016/S0168-0102(00)00124-3.
- ↑ Meyer AJ, May MJ, Fricker M (2001). «Quantitative in vivo measurement of glutathione in Arabidopsis cells.». Plant J 27 (1): 67-78. PMID 11489184. doi:10.1046/j.1365-313x.2001.01071.x.
- ↑ Meyer, A. J., Brach, T., Marty, L., Kreye, S., Rouhier, N., Jacquot, J. P. y Hell, R. (2007). «Redox-sensitive GFP in Arabidopsis thaliana is a quantitative biosensor for the redox potential of the cellular glutathione redox buffer.». Plant J 52 (5): 973-86. PMID 17892447. doi:10.1111/j.1365-313X.2007.03280.x.
Bibliografía editar
- Drevet, J. R. (mayo de 2006). "The antioxidant glutathione peroxidase family and spermatozoa: a complex story". Mol Cell Endocrinol. 250 (1-2): 70-9. doi:10.1016/j.mce.2005.12.027. PMID 16427183.
- The Role of Glutathione in Cell Defense
- Wu G, Fang YZ, Yang S, Lupton JR, Turner ND (1 March 2004). "Glutathione metabolism and its implications for health". J Nutr. 134 (3): 489–92. PMID 14988435. http://jn.nutrition.org/cgi/pmidlookup?view=long&pmid=14988435.