Reglas de Baldwin
En química orgánica, las reglas de Baldwin son un conjunto de lineamientos que delínean los favoritismos relativos de las reacciones de cierre de anillos en los compuestos alicíclicos. Fueron propuestas por primera vez por Jack Baldwin en 1976.[1][2]


Las reglas clasifican los cierres de anillo en tres formas:
- el número de átomos en nuevos anillos formados
- en cierres de anillo exo y endo, dependiendo de si el enlace roto durante el cierre del anillo está adentro (endo) o afuera (exo) del anillo que se forma
- en tet, trig y dig, dependiendo de si el carbono electrofílico es tetraédrico/sp3 (tet), trigonal/sp2, (trig) o digonal/sp, (dig)
En consecuencia, una reacción de cierre de anillo podría ser clasificada como, por ejemplo, una 5-exo-trig.
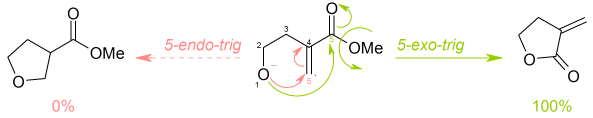
Baldwin descubrió que los requerimientos de traslape de orbitales para la formación de enlaces favorecen sólo ciertas combinaciones de tamaño de anillo y de los parámetros exo/endo/dig/trig/tet.
Existen algunas excepciones para las reglas de Baldwin. Por ejemplo, frecuentemente los cationes desobedecen las reglas de Baldwin, así como las reacciones en que está incluido en el anillo un átomo de la segunda fila. Otra excepción importante es para la ciclación 5-endo-trig, está favorecida para elementos del 2º periodo.
| Cierres de anillo des/favorecidos según Baldwin | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 3 | 4 | 5 | 6 | 7 | ||||||
| tipo | exo | end | exo | end | exo | end | exo | end | exo | end |
| tet | √ | √ | √ | X | √ | X | √ | |||
| trig | √ | X | √ | X | √ | X | √ | √ | √ | √ |
| dig | X | √ | X | √ | √ | √ | √ | √ | √ | √ |
Las reglas se aplican cuando el nucleófilo puede atacar al enlace en cuestión en un ángulo ideal. Estos ángulos son 180° para las reacciones exo-tet, 109° para las reacciones exo-trig, y 120° para las reacciones endo-dig.

Aplicaciones editar
En un estudio, se construyeron anillos de siete miembros en una reacción de adición tándem 5-exo-dig, del tipo rearreglo de Claisen:[3]
Se observó un patrón 6-endo-dig en una adición 1,2 tándem aleno - alquino del tipo ciclización de Nazarov, catalizada por un compuesto de oro:[4]
Una reacción de cierre de anillo 5-endo-dig tomó parte de una síntesis de la (+)-Preusina[5]
Las reglas de Baldwin también se aplican a las ciclizaciones aldólicas que involucran a enolatos:[6][7]
Las reglas son las siguientes:[8]
| Cierres de anillo des/favorecidos para enolatos | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| enolendo | enolexo | |||||||||
| tipo | 3 | 4 | 5 | 6 | 7 | 3 | 4 | 5 | 6 | 7 |
| exo-tet | X | X | X | √ | √ | √ | √ | √ | √ | √ |
| exo-trig | X | X | X | √ | √ | √ | √ | √ | √ | √ |
Referencias editar
- ↑ Baldwin, J. E., Rules for Ring Closure, J. Chem. Soc., Chem. Commun. 1976, 734. doi 10.1039/C39760000734(Open access)
- ↑ Baldwin, J. E., et al., Rules for Ring Closure: Ring Formation by Conjugate Addition of Oxygen Nucleophiles, J. Org. Chem., 1977, 42 (24), 3846. doi 10.1021/jo00444a011
- ↑ Li, X.; Kyne, R. E.; Ovaska, T. V. Synthesis of Seven-Membered Carbocyclic Rings via a Microwave-Assisted Tandem Oxyanionic 5-exo dig Cyclization−Claisen Rearrangement Process, J. Org. Chem., 2007, 72, 6624 doi 10.1021/jo0710432
- ↑ Guan-You Lin, Chun-Yao Yang, and Rai-Shung Liu. Gold-Catalyzed Synthesis of Bicyclo[4.3.0]nonadiene Derivatives via Tandem 6-endo-dig/Nazarov Cyclization of 1,6-Allenynes J. Org. Chem. 2007, 72, 6753-6757 doi 10.1021/jo0707939
- ↑ Overhand, Mark; Hecht, Sidney M. (1994). «A Concise Synthesis of the Antifungal Agent (+)-Preussin». The Journal of Organic Chemistry 59: 4721. doi:10.1021/jo00096a007.
- ↑ Baldwin, Jack E.; Kruse, Lawrence I. (1977). «Rules for ring closure. Stereoelectronic control in the endocyclic alkylation of ketone enolates». Journal of the Chemical Society, Chemical Communications: 233. doi:10.1039/C39770000233.
- ↑ Baldwin, J (1982). «Rules for ring closure: application to intramolecular aldol condensations in polyketonic substrates». Tetrahedron 38: 2939. doi:10.1016/0040-4020(82)85023-0.
- ↑ M. B. Smith, J. March, March’s Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, 6th ed., Wiley-Interscience, 2007, ISBN 978-0-471-72091-1