Isopreno
El isopreno o 2-metil-1,3-butadieno es un compuesto orgánico con fórmula CH2=C(CH3)-CH=CH2. A temperatura ambiente es un líquido incoloro muy volátil, debido a su bajo punto de ebullición y altamente inflamable y de fácil ignición. En contacto con el aire es altamente reactivo, capaz de polimerizarse de forma explosiva si se calienta. Es un hidrocarburo que puede dar lugar a polímeros llamados isoprenoides o terpenos.[2]
| Isopreno | ||
|---|---|---|
 | ||
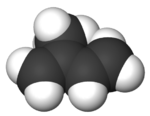 | ||
| Nombre IUPAC | ||
| 2-metilbuta-1,3-dieno | ||
| General | ||
| Otros nombres | Isopreno | |
| Fórmula semidesarrollada | CH2=C(CH3)-CH=CH2 | |
| Fórmula estructural |
 | |
| Fórmula molecular | C5H8 | |
| Identificadores | ||
| Número CAS | 78-79-5[1] | |
| ChEBI | 35194 | |
| ChEMBL | CHEMBL1566132 | |
| ChemSpider | 6309 | |
| PubChem | 6557 | |
| UNII | 0A62964IBU | |
| KEGG | C16521 | |
| Propiedades físicas | ||
| Apariencia | Líquido incoloro | |
| Densidad | 681 kg/m³; 0681 g/cm³ | |
| Masa molar | 6811 g/mol | |
| Punto de fusión | 127 K (−146 °C) | |
| Punto de ebullición | 307 K (34 °C) | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Se emplea frecuentemente en la industria y en grandes cantidades se trata de un contaminante y tóxico que puede hacer daño al medio ambiente. En algunos países como Estados Unidos el departamento de transporte considera el isopreno un material peligroso que necesita de marcas especiales.
Roles biológicos y efectos editar
El isopreno tiene un importante valor biológico por su capacidad de formar lípidos isoprenoides, moléculas lineales o cíclicas sin ácidos grasos.[2] Se elabora de forma natural en los animales y en las plantas y generalmente es el hidruro más común en el cuerpo humano. La producción estimada de isopreno en el cuerpo humano es de 15 µmol/kg/h, equivalente aproximadamente a 17 mg/día para una persona de 70 kg. El isopreno está presente también en bajas concentraciones en algunos alimentos. El isopreno se produce en algunos cloroplastos de las hojas de ciertos árboles mediante el ciclo DMAPP. La cantidad de isopreno generada por una planta depende de la masa vegetal de las hojas, su área y la luz recibida, así como de la temperatura. Durante la noche existe una pequeña emisión de isopreno mientras que de día las emisiones pueden llegar a ser sustanciales a mediodía (~5-20 mg/m²/h). Se estima la emisión mundial de isopreno por las plantas en unos 350 millones de toneladas anuales.[3]
Los lípidos de las membranas citoplasmáticas de las Arqueas poseen colas apolares, formadas por múltiples unidades de isopreno (isoprenoides), a diferencia de bacterias y eucariotas, cuyos lípidos de membrana son ácidos grasos. Estas cadenas de isoprenoides en las arqueas no forman una bicapa, sino una monocapa lipídica con largas cadenas con múltiples ramas laterales y en ocasiones anillos. Las monocapas lipídicas son muy resistentes al calor. A pesar de la diferencia entre estos dos tipos de colas, su estructura fundamental y función es la misma que la de las membranas de bacterias y eucariotas.[4]
Referencias editar
- ↑ Número CAS
- ↑ a b Biología Bachillerato. ECIR Editorial. 2006.
- ↑ «Isoprene emissions version 2021». emissions.aeronomie.be (en inglés). Consultado el 26 de septiembre de 2022.
- ↑ Madigan, Michael T. Brock. Biología de los microorganismos (14 edición). Pearson. p. 1.200. ISBN 9788490352793.
- Merck Index, Eleventh Edition, ISBN 911910-28-X ISBN 911910-28-X.
- Poisson, N., M. Kanakidou, and P. J. Crutzen, "Impact of nonmethanehydrocarbons on tropospheric chemistry and the oxidizing power of the global troposphere: 3-dimensional modelling results," Journal of Atmospheric Chemistry, vol. 36, pp. 157–230, 2000.
- Monson, R. K., and E. A. Holland, "Biospheric trace gas fluxes and their control over tropospheric chemistry," Annual Review of Ecological Systems, vol. 32, pp. 547–+, 2001.
- Claeys, M., B. Graham, G. Vas, W. Wang, R. Vermeylen, V. Pashynska, J. Cafmeyer, P. Guyon, M. O. Andreae, P. Artaxo, and W. Maenhaut, "Formation of secondary organic aerosols through photooxidation of isoprene," Science, vol. 303, pp. 1173–1176, 2004.
- Pier, P. A., and C. McDuffie, "Seasonal isoprene emission rates and model comparisons using whole-tree emissions from white oak," Journal of Geophysical Research, vol. 102, pp. 23,963–23,971, 1997.
- Poschl, U., R. von Kuhlmann, N. Poisson, and P. J. Crutzen, "Development and intercomparison of condensed isoprene oxidation mechanisms for global atmospheric modeling," Journal of Atmospheric Chemistry, vol. 37, pp. 29–52, 2000.
- Guenther, A., T. Karl, P. Harley, C. Wiedinmyer, P. I. Palmer and C. Geron, "Estimates of global terrestrial isoprene emissions using MEGAN (Model of Emissions of Gases and Aerosols from Nature)", Atmos. Chem. Phys., 6, 3181-3210, 2006. http://www.copernicus.org/EGU/acp/acp/6/3181/acp-6-3181.htm
Enlaces externos editar
- Instituto Nacional de Seguridad e Higiene en el Trabajo de España: Ficha internacional de seguridad química del isopreno.
- Flow Chart Showing the Biosynthesis of Isoprenes
- Report on Carcinogens, Eleventh Edition; U.S. Department of Health and Human Services, Public Health Service, National Toxicology Program