Micela
Se denomina micela al conjunto de moléculas que constituye una de las fases de los coloides. Es el mecanismo por el cual el jabón solubiliza las moléculas insolubles en agua, como las grasas.
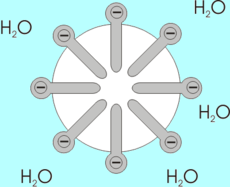
En la formación de una micela de jabón en agua, las moléculas de jabón (una sal de sodio o potasio de un ácido graso) se enlazan entre sí por sus extremos hidrófobos que corresponden a las cadenas hidrocarbonadas, mientras que sus extremos hidrófilos, aquellos que llevan los grupos carboxilo, ionizados negativamente por pérdida de un ion sodio o potasio, se repelen entre sí. De esta manera las cadenas no polares del jabón se ocultan al agua, mientras que los grupos carboxilo, cargados negativamente, se hallan expuestos a la misma.
De forma semejante, los lípidos polares en disolución acuosa diluida se dispersan formando micelas. En estas las cadenas hidrocarbonadas se ocultan del entorno acuoso y forman una fase hidrófoba interna, con los grupos hidrófilos expuestos en la superficie. Estas micelas pueden contener millares de moléculas de lípidos y, por tanto, su masa es muy elevada.
En disoluciones acuosas, las moléculas anfifílicas forman micelas en las que los grupos polares están en la superficie y las partes apolares quedan inmersas en el interior de la micela, en una disposición que elimina los contactos desfavorables entre el agua y las zonas hidrófobas y permite la solvatación de los grupos de las cadenas polares. En otro tipo de medios, las moléculas anfifílicas se pueden organizar como micelas inversas.