Ciclopropano
El ciclopropano es un anestésico por inhalación. En la práctica anestésica moderna ha sido reemplazado por otros agentes, debido a su extrema reactividad en condiciones normales: Cuando el gas se mezcla con el oxígeno hay un riesgo significativo de explosión.
| Ciclopropano | ||
|---|---|---|
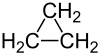    | ||
| Nombre IUPAC | ||
| Ciclopropano | ||
| General | ||
| Fórmula semidesarrollada | C3H6 | |
| Fórmula estructural | Ver imagen | |
| Fórmula molecular | C3H6 | |
| Identificadores | ||
| Número CAS | 75-19-4[1] | |
| ChEBI | 30365 | |
| ChEMBL | CHEMBL1796999 | |
| ChemSpider | 6111 | |
| DrugBank | DB13984 | |
| PubChem | 6351 | |
| UNII | 99TB643425 | |
| KEGG | D03627 | |
| Propiedades físicas | ||
| Densidad | 1879 kg/m³; 0001 g/cm³ | |
| Masa molar | 4208 g/mol | |
| Punto de fusión | 145 K (−128 °C) | |
| Punto de ebullición | 240 K (−33 °C) | |
| Peligrosidad | ||
| Límites de explosividad | 2.4% - 10.4%[2] | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Químicamente el ciclopropano es un cicloalcano cuya fórmula molecular es C3H6, que consiste de tres átomos de carbono unidos entre sí formando un anillo, y cada átomo de carbono está unido a dos átomos de hidrógeno. Es el cicloalcano más simple. Las uniones o ligaduras entre los átomos de carbono son mucho menos fuertes que una típica unión carbono-carbono. Esto se debe al ángulo de 60° entre los átomos de carbono, que es mucho menor que el ángulo normal de 109.5° de las uniones entre átomos con orbitales sp3 híbridos. La tensión en este ángulo debe ser sustraída de la energía de unión normal C-C, por lo que el compuesto químico resultante es más reactivo que un alcano acíclico y otros cicloalcanos tales como el ciclohexano y el ciclopentano.
Anestesia
editarEl ciclopropano se introdujo en uso clínico por el anestesista estadounidense Ralph Aguas que utiliza un sistema cerrado con la absorción de dióxido de carbono para conservar este agente entonces costoso. El ciclopropano es un agente de olor relativamente potente, no irritante y dulce con una concentración alveolar mínima de 17,5% y un coeficiente en sangre/gas de 0,55. Esta inducción de la anestesia por inhalación de ciclopropano y el oxígeno era rápida y no desagradable. Sin embargo, al final los pacientes con anestesia prolongada podían sufrir una disminución repentina en la presión arterial, que podía conducir a trastornos del ritmo cardíaco, una reacción conocida como "choque ciclopropano". Por esta razón, así como su elevado coste y su naturaleza explosiva, fue últimamente utilizado sólo para la inducción de la anestesia, antes de ser eliminado en gran parte.
Referencias
editar- ↑ Número CAS
- ↑ Matheson Gas Data Book. «Lower and Upper Explosive Limits for Flammable Gases and Vapors (LEL/UEL)» (en inglés). Matheson Gas Products. p. 443. Archivado desde el original el 30 de septiembre de 2019. Consultado el 2 de octubre de 2016.
Enlaces externos
editar- Molview from bluerhinos.co.uk Molécula de ciclopropano tridimensional