Sirólimus
La rapamicina o sirólimus[1] es una lactona[2] macrocíclica aislada del Streptomyces hygroscopicus, una bacteria que se encuentra en el suelo de Rapa Nui (isla de Pascua) que inhibe el crecimiento de hongos tales como Candida albicans, Microsporum gypseum y Trichophyton granulosum.[3]
| Sirólimus | ||
|---|---|---|
 | ||
 | ||
| Nombre (IUPAC) sistemático | ||
|
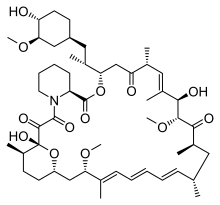
(3S,6R,7E,9R,10R,12R,14S,15E,17E,19E,21S,23S, 26R,27R,34aS)-9,10,12,13,14,21,22,23,24,25,26, 27,32,33,34,34a-hexadecahydro-9,27-dihydroxy-3- [(1R)-2-[(1S,3R,4R)-4-hydroxy-3-methoxycyclohexyl]- 1-methylethyl]-10,21-dimethoxy-6,8,12,14,20,26- hexamethyl-23,27-epoxy-3H-pyrido[2,1-c][1,4]- oxaazacyclohentriacontine-1,5,11,28,29 (4H,6H,31H)-pentone | ||
| Identificadores | ||
| Número CAS | 53123-88-9 | |
| Código ATC | L04AA10 | |
| PubChem | 6436030 | |
| Datos químicos | ||
| Fórmula | C51H79NO13 | |
| Peso mol. | 914.172 g/mol | |
| Farmacocinética | ||
| Biodisponibilidad | 20%, menos después de comidas ricas en grasa | |
| Unión proteica | 92% | |
| Metabolismo | Hepático | |
| Vida media | 57–63 horas | |
| Excreción | Principalmente fecal | |
| Datos clínicos | ||
| Cat. embarazo | C | |
| Estado legal | Venta con receta médica. | |
| Vías de adm. | Oral | |
Es un medicamento inmunosupresor usado para evitar el rechazo de órganos trasplantados; se usa especialmente en el trasplante de riñón.
Tiempo después, el medicamento mostró eficacia para combatir algunos cánceres, al frenar la proliferación celular y el crecimiento de los tumores. Por esta propiedad igualmente se utiliza para recubrir stents medicados de uso intracoronario y evitar su reestenosis.[4]
En julio de 2009, un artículo en la revista Nature demostraba que este medicamento prolongó hasta en un 38 % la vida de unos ratones,[5] hallazgo que abre expectativas sobre su utilización en tratamientos para retrasar el envejecimiento humano.
Se comercializa bajo el nombre comercial de Rapamune por Wyeth.
Historia
editarLa rapamicina que se clasifica hoy como un macrólido, fue descubierto en 1965 por un grupo de investigadores canadienses como un producto de la bacteria Streptomyces hygroscopicus en una muestra de suelo de la isla de Pascua, también conocida como “Rapa Nui”, Chile.[6][7]
Descripción
editarEl sirólimus o rapamicina es un macrólido policétido, aislado del Streptomyces hygroscopicus que ha demostrado exhibir propiedades antifúngicas, antitumorales, e inmunosupresoras.[8] La biosíntesis del núcleo del sirólimus es consumada por la enzima policétido sintasa tipo I (PKS) en conjunción con una péptido sintetasa no ribosomal. El dominio responsable para la biosíntesis del policétido del sirólimus están organizadas en tres multienzimas, RapA, RapB and RapC las cuales contiene un total de 14 módulos (Ver figura 1). Las tres multienzimas están organizadas de forma tal que el primero de los cuatro módulos de cadenas de elongación de Policétido están en RapA, los siguientes seis módulos para continuar el alargamiento están en RapB, y los últimos cuatro módulos para completar la biosíntesis del policétido linear están en RapC.[9] Entonces el policétido linear es modificado por la NRPS, RapP, la cual añade el L-pipecolate al punto final del policétido y entonces haciendo cíclica la molécula generando la molécula aislada, prerapamicin.[10]
Farmacocinética
editarFarmacodinámica
editarMecanismo de acción
editarA diferencia de su similar, el tacrolimus, el sirólimus no es un inhibidor de calcineurina. Sin embargo, tiene un efecto inmunosupresor similar sobre el sistema inmune. El sirólimus inhibe la respuesta a la interleucina-2 (IL-2) y de esa forma bloquea la activación de los linfocitos T y B. El tacrolimus además inhibe la producción de IL-2.
El mecanismo de acción del sirólimus es mediante la unión a las proteínas citosólicas FKBP12 (del inglés FK-binding protein 12) de forma similar al tacrolimus. Sin embargo, a diferencia del complejo tacrolimus/FKBP12 que inhibe la calcineurina (PP2B), el complejo sirólimus/FKBP12 inhibe la vía de la mTOR (del inglés mammalian target of rapamycin) por la unión al complejo mTOR (mTORC1). El complejo mTOR es también llamado FRAP (del inglés FKBP-rapamycin associated protein) o RAFT (del inglés rapamycin and FKBP target). La denominación FRAP y RAFT son actualmente más adecuados dado que reflejan el hecho que el sirólimus debe unirse primero al FKBP12 y solo el complejo FKBP12/rapamycin puede unirse al FRAP/RAFT/mTOR.
mTOR es una serina/treonina proteína cinasa que regula el crecimiento, la proliferación, la motilidad y la supervivencia celulares, además de la síntesis de proteínas y la transcripción.[11][12]
Uso clínico
editarUso en trasplantes
editarLa principal ventaja que el sirólimus tiene sobre los inhibidores de calcineurina, es la de tener baja toxicidad renal. Los pacientes trasplantados en tratamiento con inhibidores de calcineurina a largo plazo tienden a perder función renal e incluso llegar a la falla renal terminal; esto puede evitarse con el uso del sirólimus. Es particularmente ventajoso en pacientes trasplantados a causa del síndrome urémico hemolítico, ya que esta enfermedad es probable que recurra en el riñón trasplantado si es usado un inhibidor de calcineurina. Sin embargo, el 7 de octubre de 2008, la FDA aprobó una marca de revisión de la seguridad del sirólimus para advertir del riesgo de disminución de la función renal con su uso.
El sirólimus puede ser utilizado solo o en combinación con inhibidores de la calcineurina y/o micofenolato, proveyendo así regímenes de inmunosupresión libres de esteroides. Sin embargo, disminución en la curación de heridas y trombocitopenia es un posible efecto colateral del sirólimus, por ello muchos centros de trasplante prefieren no utilizarlo inmediatamente después de la operación de trasplante, en lugar de ello es administrado solo después de un periodo de semanas o meses. Su desempeño óptimo como inmunosupresor todavía no ha sido determinado, y es sujeto de una cantidad de ensayos clínicos en desarrollo.
Efectos adversos
editarToxicidad sobre pulmón
editarLa toxicidad pulmonar es una importante complicación derivada del uso de sirólimus, sobre todo en los pacientes sometidos a trasplante de pulmón.[13][14][15][16][17][18][19][20]
El mecanismo de acción de este efecto adverso no está totalmente aclarado.[21][22][23] La neumonitis intersticial ocasionada en ocasiones por el medicamento no es dependiente de la dosis.[13][24]
Investigación
editarIncremento de la esperanza de vida en ratones
editarEn un estudio de 2009, la esperanza de vida de ratones recibiendo sirólimus se incrementó entre 28-38 % desde el inicio del tratamiento, o 9-14 % en total de incremento en la esperanza de vida máxima. Es de notar que el tratamiento se inició en ratones de 20 meses, el equivalente a 60 años humanos. Esto sugiere la posibilidad de un tratamiento anti envejecimiento efectivo para humanos en edad ya avanzada, sin requerir un tratamiento a largo plazo desde la juventud.[25] Sin embargo, debido a la fuerte supresión del sistema inmune, el medicamento no puede ser fácilmente usado en humanos. Mientras que los ratones estaban confinados en un medio libre de patógenos, los humanos tomando sirólimus son muy susceptibles a las infecciones en forma permanente, requiriendo supervisión médica permanente.[26]
Efectos anti proliferativos
editarLos efectos antiproliferativos del sirólimus han sido usados en el contexto de los stents coronarios para prevenir la estenosis de las arterias coronarias posterior a la angioplastia con balón. El sirólimus es prescrito en una capa polimérica que permite la liberación prolongada durante el periodo de cicatrización posterior a la intervención coronaria.
Algunos estudios clínicos extensos han demostrado tasas bajas de reestenosis en pacientes tratados con stens liberadores de sirólimus, comparado con aquellos de metal desnudo, resultando en menos reintervenciones. Un estent coronario liberador de sirólimus es comercializado por Cordis, una división de Johnson & Johnson, bajo el nombre comercial de 'Cypher'.[27] Ha sido propuesto, sin embargo, que tales stens pueden incrementar el riesgo de trombosis vascular.[28]
En forma adicional, el sirólimus actualmente está siendo sugerido como una opción terapéutica para la enfermedad poliquística renal autosómica dominante. Casos reportados indican que el sirólimus puede reducir el volumen renal y demorar la pérdida de función renal en pacientes con esta patología,[29] de igual forma algunos estudios están evaluando su eficacia como opción en el tratamiento de la fibrosis pulmonar.[30]
Esclerosis tuberosa
editarEl sirólimus también es promisorio en el tratamiento de la esclerosis tuberosa, un desorden congénito en el cual existe una propensión al crecimiento de tumores benignos en el cerebro, corazón, riñones, piel y otros órganos. Después de algunos estudios se relacionó en forma conclusiva los inhibidores de mTOR a la remisión de tumores en la esclerosis tuberosa, específicamente astrocitomas subependimarios de células gigantes en niños y angiolipomas en adultos, muchos médicos en los EE. UU. empezaron a prescribir el sirólimus a pacientes con esclerosis tuberosa sin estar aprobado por la FDA. Numerosos estudios clínicos utilizando sirólimus y análogos, involucrando adultos y niños con esclerosis tuberosa, se encuentran en curso en los Estados Unidos.[31]
La mayoría de los estudios han mostrado claramente que los tumores a menudo recidivan cuando el tratamiento es suspendido. Se teoriza que el medicamento aminoras los síntomas de la esclerosis tuberosa, como los angiofibromas faciales TDAH, y autismo, son un tema de investigación actual en modelos animales.
Cáncer
editarLos efectos antiproliferativos del sirólimus pueden tener un rol en el tratamiento del cáncer. Recientemente se demostró que el sirólimus inhibía la progresión del Sarcoma de Kaposi en pacientes con trasplante renal. Otros inhibidores de la mTOR tales como el temsirólimus (CCI-779) o everolimus (RAD001) están siendo probados para su uso en cánceres como el glioblastoma multiforme y linfoma de células de manto.
La combinación de doxorrubicina y sirólimus ha demostrado llevar los linfomas AKT positivos a la remisión en ratones. Las señales mediadas por las Akt promueven la supervivencia celular en linfomas Akt positivos y actúa previniendo los efectos citotóxicos de los fármacos quimioterapéuticos como la doxorrubicina o ciclofosfamida. El sirólimus bloquea las señales de las Akt y las células pierden la resistencia a la quimioterapia. Los linfomas positivos para Bcl-2 fueron completamente resistentes a la terapia; no como los linfomas que expresan eIF4E y son sensibles al sirólimus.[32][33][34][35]
El panobinostat ha demostrado actuar sinérgicamente con el sirólimus para matar células pancreáticas en el laboratorio, en un estudio de la clínica Mayo. En el mencionado estudio, los investigadores encontraron que esta combinación destruía hasta el 65 % de las células pancreáticas tumorales cultivadas. El hallazgo es significativo porque las tres líneas celulares estudiadas eran todas resistentes a los efectos de la quimioterapia, como la mayoría de los tumores pancreáticos.[36]
Como con todos los medicamentos inmunosupresores, el sirólimus disminuye la actividad anti oncogénica del organismo y permite la proliferación de algunos cánceres, los cuales serían normalmente destruidos. Los pacientes inmunosuprimidos, tiene un riesgo de cáncer de 10 a 100 veces más alto que la población general. Además, los pacientes quienes actualmente tienen o han sido tratados para el cáncer, tienen una alta tasa más alta de probabilidad de progresión del tumor y recurrencia que los pacientes con un sistema inmune intacto.
Véase también
editarReferencias
editar- ↑ Real Academia Nacional de Medicina. «Sirólimus». dtme.ranm.es. Consultado el 18 de julio de 2021.
- ↑ «SIROLIMUS EN VADEMECUM». www.iqb.es. Consultado el 25 de agosto de 2020.
- ↑ Tee, Andrew R. (marzo de 2018). «The Target of Rapamycin and Mechanisms of Cell Growth» [El blanco de la rapamicina y mecanismos del crecimiento celular]. Int J Mol Sci (en inglés) 19 (3): 880. PMID 29547541. doi:10.3390/ijms19030880. Consultado el 25 de octubre de 2018.
- ↑ Regara, Evelyn. Serruysa, Patrick W.El estudio RAVEL. Reestenosis del cero por ciento: ¡un sueño del cardiólogo hecho realidad. Rev Esp Cardiol. 2002;55:459-62. [1]
- ↑ Harrison, David E. et al. Rapamycin fed late in life extends lifespan in genetically heterogeneous mice. Nature 460, 392-395 (16 July 2009)| doi:10.1038/nature08221.[2].
- ↑ Fuster, Valentín (2003). «La rapamicina: del laboratorio al tratamiento de las arterias en los pacientes». Rev Esp Cardiol 56 (Supl 1): 2-6. PMID 15626356. Consultado el 25 de octubre de 2018.
- ↑ Vézina, Claude; Kudelski, Alicia; Sehgal, S. N. (octubre de 1975). «Rapamycin (AY-22,989), a new antifungal antibiotic. I. Taxonomy of the producing streptomycete and isolation of the active principle» [Rapamicina (AY-22,989), un nuevo antibiótico antifúngico. Taxonomía del estreptomiceto que lo produce y aislamiento del principio activo]. J Antibiot (Tokyo) (en inglés) (Quebec, Canadá) 28 (10): 721-726. PMID 1102508. Consultado el 25 de octubre de 2018.
- ↑ Vézina C, Kudelski A, Sehgal SN (octubre de 1975). «Rapamycin (AY-22,989), a new antifungal antibiotic.». J. Antibiot. 28 (10): 721-6. PMID 1102508.
- ↑ Schwecke T, Aparicio JF, Molnár I, et al. (agosto de 1995). «The biosynthetic gene cluster for the polyketide immunosuppressant rapamycin». Proc. Natl. Acad. Sci. U.S.A. 92 (17): 7839-43. PMC 41241. PMID 7644502. doi:10.1073/pnas.92.17.7839. Consultado el 8 de julio de 2009.
- ↑ Gregory MA, Gaisser S, Lill RE, et al. (mayo de 2004). «Isolation and characterization of pre-rapamycin, the first macrocyclic intermediate in the biosynthesis of the immunosuppressant rapamycin by S. hygroscopicus». Angew. Chem. Int. Ed. Engl. 43 (19): 2551-3. PMID 15127450. doi:10.1002/anie.200453764.
- ↑ Hay N, Sonenberg N (2004). «Upstream and downstream of mTOR». Genes Dev 18 (16): 1926-45. PMID 15314020. doi:10.1101/gad.1212704.
- ↑ Beevers C, Li F, Liu L, Huang S (2006). «Curcumin inhibits the mammalian target of rapamycin-mediated signaling pathways in cancer cells». Int J Cancer 119 (4): 757-64. PMID 16550606. doi:10.1002/ijc.21932.
- ↑ a b Chhajed PN, Dickenmann M, Bubendorf L, Mayr M, Steiger J, Tamm M (2006). «Patterns of pulmonary complications associated with sirolimus». Respiration 73 (3): 367-74. PMID 16127266. doi:10.1159/000087945.
- ↑ Morelon E, Stern M, Israël-Biet D, et al. (septiembre de 2001). «Characteristics of sirolimus-associated interstitial pneumonitis in renal transplant patients». Transplantation 72 (5): 787-90. PMID 11571438. doi:10.1097/00007890-200109150-00008.
- ↑ Filippone EJ, Carson JM, Beckford RA, et al. (septiembre de 2011). «Sirolimus-induced pneumonitis complicated by pentamidine-induced phospholipidosis in a renal transplant recipient: a case report». Transplant. Proc. 43 (7): 2792-7. PMID 21911165. doi:10.1016/j.transproceed.2011.06.060.
- ↑ Pham PT, Pham PC, Danovitch GM, et al. (abril de 2004). «Sirolimus-associated pulmonary toxicity». Transplantation 77 (8): 1215-20. PMID 15114088. doi:10.1097/01.TP.0000118413.92211.B6. Archivado desde el original el 7 de junio de 2012. Consultado el 28 de junio de 2015.
- ↑ Mingos MA, Kane GC (diciembre de 2005). «Sirolimus-induced interstitial pneumonitis in a renal transplant patient». Respir Care 50 (12): 1659-61. PMID 16318648. Archivado desde el original el 22 de julio de 2012. Consultado el 28 de junio de 2015.
- ↑ Das BB, Shoemaker L, Subramanian S, Johnsrude C, Recto M, Austin EH (marzo de 2007). «Acute sirolimus pulmonary toxicity in an infant heart transplant recipient: case report and literature review». J. Heart Lung Transplant. 26 (3): 296-8. PMID 17346635. doi:10.1016/j.healun.2006.12.004.
- ↑ Delgado JF, Torres J, José Ruiz-Cano M, et al. (septiembre de 2006). «Sirolimus-associated interstitial pneumonitis in 3 heart transplant recipients». J. Heart Lung Transplant. 25 (9): 1171-4. PMID 16962483. doi:10.1016/j.healun.2006.05.013.
- ↑ McWilliams TJ, Levvey BJ, Russell PA, Milne DG, Snell GI (febrero de 2003). «Interstitial pneumonitis associated with sirolimus: a dilemma for lung transplantation». J. Heart Lung Transplant. 22 (2): 210-3. PMID 12581772. doi:10.1016/S1053-2498(02)00564-8.
- ↑ Aparicio G, Calvo MB, Medina V, et al. (agosto de 2009). «Comprehensive lung injury pathology induced by mTOR inhibitors». Clin Transl Oncol 11 (8): 499-510. PMID 19661024. doi:10.1007/s12094-009-0394-y.
- ↑ Paris A, Goupil F, Kernaonet E, et al. (enero de 2012). «[Drug-induced pneumonitis due to sirolimus: an interaction with atorvastatin?]». Rev Mal Respir (en francés) 29 (1): 64-9. PMID 22240222. doi:10.1016/j.rmr.2010.03.026.
- ↑ Maroto JP, Hudes G, Dutcher JP, et al. (mayo de 2011). «Drug-related pneumonitis in patients with advanced renal cell carcinoma treated with temsirolimus». J. Clin. Oncol. 29 (13): 1750-6. PMID 21444868. doi:10.1200/JCO.2010.29.2235. Archivado desde el original el 15 de abril de 2013. Consultado el 28 de junio de 2015.
- ↑ Errasti P, Izquierdo D, Martín P, et al. (octubre de 2010). «Pneumonitis associated with mammalian target of rapamycin inhibitors in renal transplant recipients: a single-center experience». Transplant. Proc. 42 (8): 3053-4. PMID 20970608. doi:10.1016/j.transproceed.2010.07.066.
- ↑ Harrison DE, Strong R, Sharp ZD, et al. (8 de julio de 2009). «Rapamycin fed late in life extends lifespan in genetically heterogeneous mice». Nature. doi:10.1038/nature08221. Resumen divulgativo – London Times (8 de julio de 2009).
- ↑ Jocelyn Rice (8 de julio de 2009). «First Drug Shown to Extend Life Span in Mammals». Technology Review (Massachusetts Institute of Technology): 1-2. Archivado desde el original el 12 de septiembre de 2011. Consultado el 9 de julio de 2009.
- ↑ «Cypher Sirolimus-eluting Coronary Stent». Cypher Stent. Archivado desde el original el 23 de noviembre de 2008. Consultado el 1 de abril de 2008.
- ↑ Shuchman M (2006). «Trading restenosis for thrombosis? New questions about drug-eluting stents». N Engl J Med 355 (19): 1949-52. PMID 17093244. doi:10.1056/NEJMp068234.
- ↑ Peces R, Peces C, Pérez-Dueñas V, et al. (16 de enero de 2009). «Rapamycin reduces kidney volume and delays the loss of renal function in a patient with autosomal-dominant polycystic kidney disease». NDT Plus (Oxford Journals) 2 (2): 133-135. ISSN 1753-0792. doi:10.1093/ndtplus/sfn210.
- ↑ Rondón, Carlos (14 de diciembre de 2011). «Rapamune muestra efectividad antifibrótica». Consultado el 1 de enero de 2012.
- ↑ Tuberous Sclerosis Alliance (octubre de 2009). Current Clinical Trials. Archivado desde el original el 22 de enero de 2009. Consultado el 14 de octubre de 2009.
- ↑ Sun SY, Rosenberg LM, Wang X, et al. (agosto de 2005). «Activation of Akt and eIF4E survival pathways by rapamycin-mediated mammalian target of rapamycin inhibition». Cancer Res. 65 (16): 7052-8. PMID 16103051. doi:10.1158/0008-5472.CAN-05-0917. Consultado el 8 de julio de 2009.
- ↑ Chan S (2004). «Targeting the mammalian target of rapamycin (mTOR): a new approach to treating cancer». Br J Cancer 91 (8): 1420-4. PMC 2409926. PMID 15365568. doi:10.1038/sj.bjc.6602162.
- ↑ Wendel HG, De Stanchina E, Fridman JS, et al. (marzo de 2004). «Survival signalling by Akt and eIF4E in oncogenesis and cancer therapy». Nature 428 (6980): 332-7. PMID 15029198. doi:10.1038/nature02369. Resumen divulgativo – ScienceDaily (18 de marzo de 2004).
- ↑ Novak, Kristine (mayo de 2004). «Therapeutics: Means to an end». Nature Reviews Cancer 4: 332. doi:10.1038/nrc1349. Archivado desde el original el 10 de febrero de 2008. Consultado el 8 de julio de 2009.
- ↑ «Mayo Clinic Researchers Formulate Treatment Combination Lethal To Pancreatic Cancer Cells». Archivado desde el original el 20 de febrero de 2012. Consultado el 22 de junio de 2010.