Sustancias poliméricas extracelulares
Las sustancias poliméricas extracelulares, SPEs (del inglés Extracellular Polymeric Substances, EPSs) son los polímeros naturales de alto peso molecular secretados por microorganismos a su entorno.[1] Las SPEs constituyen la integridad funcional y estructural de los biofilms, y se consideran el componente fundamental que determina las características fisioquímicas de un biofilm.[2]
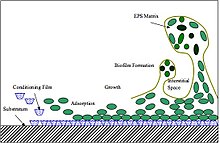
Las SPEs están principalmente compuestos por polisacáridos (exopolisacáridos) y proteínas, pero incluyen también otras macromoléculas, como ADN, lípidos y sustancias húmicas. Los SPEs son el material con el que se llevan a cabo los asentamiento bacterianos y pueden permanecer unidos a la superficie celular externa o ser secretados al medio de crecimiento. Estos compuestos son importantes en la formación de biofilms y en la unión de las células a las superficiees. Los SPEs constituyen de un 50% a un 90% de la materia orgánica total de los biofilms.[2][3][4]
Los exopolisacáridos (abreviados como SPEs en español y EPSs en inglés) son polímeros de alto peso molecular compuestos de residuos de azúcares que son secretados por un microorganismo al medio circundante. Los microorganismos sintetizan un amplio abanico de polisacáridos multifuncionales que incluyen polisacáridos intracelulares, polisacáridos estructurales y polisacáridos extracelulares o exopolisacáridos. Los exopolisacáridos constan generalmente de monosacáridos y algunos sustituyentes no glucídicos (como acetato, piruvato, succinato y fosfato). Debido a la amplia diversidad en cuanto a su composición, los exopolisacáridos poseen diversas aplicaciones en industrias como la alimentaria o la farmacéutica. Algunos SPEs otorgan propiedades que son muy similares o casi idénticas a las de las gomas (como la goma xantana) que se emplean actualmente en estas industrias. Actualmente se están llevando a cabo esfuerzos para reemplazar las gomas procedentes de plantas y algas empleadas tradicionalmente por su equivalente microbiano. Además, se ha realizado un progreso considerable en el descubrimiento y desarrollo de nuevos SPE microbianos con relevancia industrial.[5]
Función
editarLos exopolisacáridos capsulares pueden proteger a bacterias patogénicas contra la desecación y la predación, y contribuye a su patogenecidad.[6] Las bacterias existentes en los biofilms son menos vulnerables en comparación con bacterias planctónicas, puesto que la matriz de SPEs es capaz de actuar como una barrera protectora frente a la difusión.[7] Las características físicas y químicas de las células bacterianas pueden verse afectadas por la composición de los SPEs, lo que puede influir en factores como el reconocimiento celular, la agregación y la adhesión de las bacterias en sus ambientes naturales.[7] Además, la capa de SPE actúa como una trampa para los nutrientes, facitlitando el crecimiento bacteriano.[7]
Los exopolisacáridos de algunas cepas de bacterias ácido lácticas, como Lactococcus lactis subsp. cremoris, contribuyen a la textura gelatinosa de productos lácteos fermentados y son también digeribles.[8][9] Un ejemplo de uso industrial de estos exopolisacáridos es la aplicación de dextrano en panetones y otros panes de la industria panadera.[10]
Ecología
editarLos exopolisacáridos pueden facilitar la unión de bacterias fijadoras de nitrógeno a las raíces de las plantas y partículas del suelo, estableciéndose una relación simbiótica.[11] Este fenómeno es importante para la colonización de las raíces y la rizosfera, que es un componente clave de redes tróficas del suelo y los ciclos de nutrientes en los ecosistemas. Permite además una exitosa invasión e infección de la planta hospedadora.[11]
Las sustancias poliméricas extracelulares bacterianas pueden participar en procesos de biorremediación de metales pesados en tanto que poseen la capacidad de adsorber cationes metálicos, entre otras sustancias disueltas.[12] Esto resulta útil en sistemas de tratamiento de aguas residuales, ya que los biofilms con capaces de unir y eliminar metales tales como el cobre, níquel, cadmio y plomo.[12] La afinidad de la unión y la especificidad de metal de los SPEs varían dependiendo de la composición polimérica, así como de factores ambientales como la concentración y el pH.[12]
En un contexto geomicrobiológico, se ha observado que los SPEs afectan a la precipitación de minerales, particularmente carbonatos.[13] También pueden unir y atrapar partículas en suspensiones de biofilms, lo que puede restringir la dispersión y el ciclo de los elementos.[13] La estabilidad delos sedimentos puede incrementarse mediante los SPEs, ya que estos influencian la cohesión, la permeabilidad y la erosión del sedimento.[13] Existe evidencia de que la adhesión y la capacidad de unir metales de los SPEs afectan los índices de lixiviación mineral tanto en un contexto ambiental como industrial.[13] Estas interacciones entre los SPEs y el entorno abiótico permite el amplio impacto de los SPEs en los ciclos biogeoquímicos.
Uso industrial novedosos
editarDebido a la creciente necesidad de encontrar una alternativa más eficaz y respetuosa con el medio ambiente respecto a los actuales métodos convencionales de eliminación de residuos, las industrias están haciendo cada vez más hincapié a la función de las bacterias y sus SPEs en procesos de biorremediación.[14]
Algunos investigadores han encontrado que la adición de SPEs de cianobacterias a aguas residuales elimina metales pesado como el cobre, cadmio y plomo.[14] Los SPEs pueden interaccionar físicamente con estos metales pesados y retenerlos mediante bioadsorción.[14] La eficiencia del proceso de extracción puede ser optimizada mediante el tratamiento de los SPEs con diferentes tipos de ácidos o bases antes de añadirlos a las aguas residuales.[14]
Los suelos contaminados contiene elevados niveles de hidrocarburos aromáticos policíclicos (HAPs). Los SPEs de dos bacterias, Zoogloea sp. y Aspergillus niger, son efectivos eliminando estos compuestos tóxicos.[15] Los SPEs contienen también enzimas como oxidorreductasas e hidrolasas, las cuales son capaces de degradar los HAPs.[15] La cantidad de HAPs degradado depende de la concentración de SPEs añadida al suelo. Este método ha demostrado ser relativamente barato y de alta eficiencia.[15]
En los últimos años, los SPEs de bacterias marinas han sido empleados en la limpieza de vertidos petrolíferos.[16] Durante el desastre de la plataforma petrolífera Deepwater Horizon en 2010, estas bacterias productoras de SPEs demostraron ser capaces de crecer y proliferar rápidamente.[16] Más tarde se encontró que los SPEs disolvieron el crudo y formaron agregados en la superficie del océano, lo que contribuyó a acelerar el proceso de limpieza del vertido.[16] Estos agregados también proporcionaron un valiosa fuente de nutrientes para otras comunidades microbianas marinas. Estos conjuntos de aceite también proporcionados una fuente valiosa de nutrientes para otras comunidades microbianas marinas. Esto ha permitido a los científicos modificar y optimizar el uso de los SPEs para la limpieza de este tipo de vertidos.[16]
Lista
editar- acetano (Acetobacter xylinum)
- alginato(Azotobacter vinelandii)
- celulosa (Acetobacter xylinum)
- quitosán (Mucorales spp.)
- curdlan (Alcaligenes faecalis var. myxogenes)
- ciclosoforanos (Agrobacterium spp., Rhizobium spp. Y Xanthomonas spp.)
- dextrano (Leuconostoc mesenteroides, Leuconostoc dextranicum y Lactobacillus hilgardii)
- emulsan (Acinetobacter calcoaceticus)
- galactoglucopolisacaráidos (Achromobacter spp., Agrobacterium radiobacter, Pseudomonas marginalis, Rhizobium spp. Y Zooglea' spp.)
- galactosaminogalactano (Aspergillus spp.)
- gelan (Aureomonas elodea Y Sphingomonas paucimobilis)
- glucuronan (Sinorhizobium meliloti)
- N-acetilglucosamina (Staphylococcus epidermidis)
- N-acetil-heparosan (Escherichia coli)
- ácido hialurónico (Estreptococo equi)
- indicán (Beijerinckia indica)
- kefiran (Lactobacillus hilgardii)
- lentinano (Lentinus elodes)
- levano (Alcaligenes viscosus, Zymomonas mobilis, Bacilo subtilis)
- pululano (Aureobasidium pullulans)
- escleroglucano (Sclerotium rolfsii, Sclerotium delfinii y Sclerotium glucanicum)
- escizofilano (Schizophylum Comuna)
- stewartan (Pantoea stewartii subsp. stewartii)
- succinoglucano (Alcaligenes faecalis var myxogenes, Sinorhizobium meliloti)
- xantano (Xanthomonas campestris)
- welano (Alcaligenes spp.)
Véase también
editar- Matriz extracelular en organismos multicelulares.
Referencias
editar- ↑ «Volumetric measurements of bacterial cells and extracellular polymeric substance glycoconjugates in biofilms». Biotechnol. Bioeng. 88 (5): 585-92. 2004. PMID 15470707. doi:10.1002/bit.20241.
- ↑ a b Flemming, Hans-Curt; Wingender, Jost; Griebe, Thomas; Mayer, Christian (21 de diciembre de 2000), «Physico-Chemical Properties of Biofilms», en L. V. Evans, ed., Biofilms: Recent Advances in their Study and Control, CRC Press, p. 20, ISBN 978-9058230935.
- ↑ Donlan RM (2002). «Biofilms: microbial life on surfaces». Emerging Infect. Dis. 8 (9): 881-90. PMC 2732559. PMID 12194761. doi:10.3201/eid0809.020063.
- ↑ «Biofilms: survival mechanisms of clinically relevant microorganisms». Clin. Microbiol. Rev. 15 (2): 167-93. 2002. PMC 118068. PMID 11932229. doi:10.1128/CMR.15.2.167-193.2002.
- ↑ Suresh and Mody (2009). «Microbial Exopolysaccharides: Variety and Potential Applications». Microbial Production of Biopolymers and Polymer Precursors. Caister Academic Press. ISBN 978-1-904455-36-3.
- ↑ Ghosh, Pallab Kumar; Maiti, Tushar Kanti (2016). «Structure of Extracellular Polysaccharides (EPS) Produced by Rhizobia and their Functions in Legume–Bacteria Symbiosis: — A Review». Achievements in the Life Sciences 10 (2): 136-143. doi:10.1016/j.als.2016.11.003.
- ↑ a b c Harimawan, Ardiyan; Ting, Yen-Peng (1 de octubre de 2016). «Investigation of extracellular polymeric substances (EPS) properties of P. aeruginosa and B. subtilis and their role in bacterial adhesion». Colloids and Surfaces B: Biointerfaces 146 (Supplement C): 459-467. doi:10.1016/j.colsurfb.2016.06.039.
- ↑ Welman AD (2009). «Exploitation of Exopolysaccharides from lactic acid bacteria». Bacterial Polysaccharides: Current Innovations and Future Trends. Caister Academic Press. ISBN 978-1-904455-45-5.
- ↑ Ljungh A, Wadstrom T (editors) (2009). Lactobacillus Molecular Biology: From Genomics to Probiotics. Caister Academic Press. ISBN 978-1-904455-41-7.
- ↑ Ullrich M (editor) (2009). Bacterial Polysaccharides: Current Innovations and Future Trends. Caister Academic Press. ISBN 978-1-904455-45-5.
- ↑ a b Ghosh, Pallab Kumar; Maiti, Tushar Kanti (2016). «Structure of Extracellular Polysaccharides (EPS) Produced by Rhizobia and their Functions in Legume–Bacteria Symbiosis: — A Review». Achievements in the Life Sciences 10 (2): 136-143. doi:10.1016/j.als.2016.11.003.
- ↑ a b c Pal, Arundhati; Paul, A. K. (1 de marzo de 2008). «Microbial extracellular polymeric substances: central elements in heavy metal bioremediation». Indian Journal of Microbiology (en inglés) 48 (1): 49-64. ISSN 0046-8991. PMC 3450203. PMID 23100700. doi:10.1007/s12088-008-0006-5.
- ↑ a b c d Tourney, Janette; Ngwenya, Bryne T. (29 de octubre de 2014). «The role of bacterial extracellular polymeric substances in geomicrobiology». Chemical Geology 386 (Supplement C): 115-132. doi:10.1016/j.chemgeo.2014.08.011.
- ↑ a b c d Mota, Rita; Rossi, Federico; Andrenelli, Luisa; Pereira, Sara Bernardes; De Philippis, Roberto (September 2016). «Released polysaccharides (RPS) from Cyanothece sp. CCY 0110 as biosorbent for heavy metals bioremediation: interactions between metals and RPS binding sites.». Applied Microbiology and Biotechnology 100 (17): 7765-7775. PMID 27188779. doi:10.1007/s00253-016-7602-9.
- ↑ a b c Jia, Chunyun; Li, Peijun; Li, Xiaojun; Tai, Peidong; Liu, Wan; Gong, Zongqiang (1 de agosto de 2011). «Degradation of pyrene in soils by extracellular polymeric substances (EPS) extracted from liquid cultures». Process Biochemistry 46 (8): 1627-1631. doi:10.1016/j.procbio.2011.05.005.
- ↑ a b c d Gutierrez, Tony; Berry, David; Yang, Tingting; Mishamandani, Sara; McKay, Luke; Teske, Andreas; Aitken, Michael D. (27 de junio de 2013). «Role of Bacterial Exopolysaccharides (EPS) in the Fate of the Oil Released during the Deepwater Horizon Oil Spill». PLOS ONE 8 (6): e67717. ISSN 1932-6203. PMID 23826336. doi:10.1371/journal.pone.0067717.